题目内容
【题目】日常生活中所说的盐,通常指食盐(主要成分是氯化钠)。
(1)氯化钠是由___________(写粒子符号)构成的;
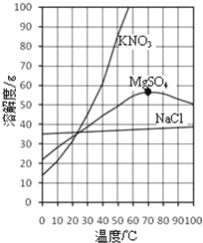
(2)通过晾晒海水,可以蒸发除去水分,得到粗盐。通常不采用降低海水温度的方法得到粗盐,是因为_________________________________,相同情况下降温析出的晶体比较少;
(3)根据“粗盐中难溶性杂质的去除”实验,回答有关问题:
①溶解 称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.1g。
②过滤
③蒸发 在加热过程中,用玻璃棒不断搅拌,防止______________________________________。当蒸发皿中______________________,停止加热。
④计算产率 得到精盐3.3g,则精盐的产率为___________(计算结果保留一位小数)。
(4)若经过上述实验得到的精盐中还含有氯化镁、氯化钙,为了除去这两种可溶性杂质,可将得到的精盐全部溶于水,加入过量的氢氧化钠溶液和___________________溶液,充分反应后,接下来的操作顺序是__________________(填序号)。
①蒸发 ②加入过量的稀盐酸 ③过滤
【答案】 Na+、Cl— NaCl溶解度受温度变化的影响很小 局部温度过高,导致液滴飞溅 出现较多固体 84.6% Na2CO3 ③②①
【解析】(1)根据物质的构成分析;
(2)根据氯化钠的溶解度受温度影响变化较小分析;
(3)③根据蒸发过程中玻璃棒的作用及蒸发时停止加热的时间分析;
④根据精盐与所溶解的粗盐的质量比解答;
(4)根据粗盐中可溶性杂质的去处方法分析。
解:(1)氯化钠是离子化合物,故氯化钠是由Na+、Cl—构成的;
(2)实验中不采用降低海水温度的方法得到粗盐,是因为氯化钠的溶解度受温度影响变化较小,相同情况下降温析出的晶体比较少;
(3)③在加热过程中,用玻璃棒不断搅拌,防止局部温度过高,导致液滴飞溅。当蒸发皿中出现较多固体,停止加热;
④![]() =84.6%;
=84.6%;
(4)加入过量的氢氧化钠溶液除去氯化镁的杂质,要除去氯化钙必须加入过量的Na2CO3溶液,然后过滤除去生成的氢氧化镁、碳酸钙,再加入过量的稀盐酸除去
过量的氢氧化钠溶液和过量的稀盐酸,最后蒸发结晶。故填Na2CO3 ③②①。