题目内容
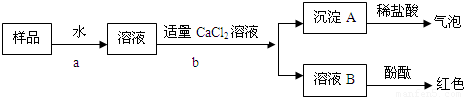
(2010?绵阳)(1)图Ⅰ、图Ⅱ是研究燃烧的条件的装置,试分析后填空:图Ⅰ实验是利用不同物质在条件下燃烧和不燃烧,来证实可燃物燃烧所需的条件之一:温度达到着火点.
仅用图Ⅱ所示装置就可以证实可燃物必须与氧气(或空气)接触才能燃烧,其做法是:.
(2)我省有着丰富的天然气资源,许多化肥厂用天然气在高温、催化剂作用下与水蒸气反应来制备氢气和一氧化碳:CH4+H2O
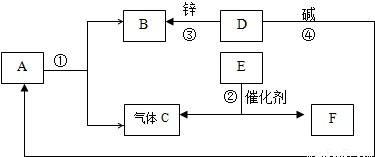
 CO+3H2.为了证实该反应所生成的混合气体的成分,兴趣小组的同学设计了如下图所示装置并进行实验,请你回答下列相关问题:
CO+3H2.为了证实该反应所生成的混合气体的成分,兴趣小组的同学设计了如下图所示装置并进行实验,请你回答下列相关问题:【实验目的】证实混合气体中含有CO和H2

【进行实验】在装置中通入混合气体,点燃酒精灯,如上图所示进行实验
【实验分析】①若要证实混合气体中有CO,应该观察到的现象是,相关的化学反应方程式是.
②若要证实混合气体中有H2,且是通过装置B验证的,应采用的方法是.
③有同学认为,根据该混合气体生产的实际情况,混合气体中可能含有水分,因而还应对上述实验装置加以改进.请你提出改进的方案.

【答案】分析:(1)根据装置和药品分析出相同的条件,仅用图Ⅱ所示装置就可以证实可燃物必须与氧气(或空气)接触才能燃烧,要考虑能形成对照实验;
(2)①根据一氧化碳的验证方法考虑,具有还原性并且能生成二氧化碳考虑;②根据氢气的性质和反应产物考虑;③用一药品将混合气体中可能含有水分除掉.
解答:解:(1)白磷、红磷着火点不同,可燃物种类不同,但热水的温度相同,在第二个装置中需形成对照实验,通入氧气白磷燃烧,停止通氧气白磷熄灭,就形成了对照试验;
(2)①由于一氧化碳具有还原性,能使氧化铜变成铜,并生成二氧化碳,所以现象是黑色氧化铜变成红色,石灰水变浑浊,方程式有两个:一氧化碳还原氧化铜生成铜和二氧化碳,二氧化碳与石灰水反应生成碳酸钙和水;②由于氢气还原氧化铜生成了铜和水,浓硫酸具有吸水性,浓硫酸质量的增加量就是生成水的质量.③在A装置前放一除水装置(例如用浓硫酸).
故答案为:(1)相同温度;间歇通入氧气;(2)①石灰水变浑浊,A中黑色粉末变为红色;CO+CuO Cu+CO2;CO2+Ca(OH)2=CaCO3↓+H2O②称量反应前后装置B的质量并进行比较③在装置A前增加除水分装置.
Cu+CO2;CO2+Ca(OH)2=CaCO3↓+H2O②称量反应前后装置B的质量并进行比较③在装置A前增加除水分装置.
点评:通过回答本题知道了验证燃烧条件的对照实验的设计方法,掌握了氢气和一氧化碳的验证方法.
(2)①根据一氧化碳的验证方法考虑,具有还原性并且能生成二氧化碳考虑;②根据氢气的性质和反应产物考虑;③用一药品将混合气体中可能含有水分除掉.
解答:解:(1)白磷、红磷着火点不同,可燃物种类不同,但热水的温度相同,在第二个装置中需形成对照实验,通入氧气白磷燃烧,停止通氧气白磷熄灭,就形成了对照试验;
(2)①由于一氧化碳具有还原性,能使氧化铜变成铜,并生成二氧化碳,所以现象是黑色氧化铜变成红色,石灰水变浑浊,方程式有两个:一氧化碳还原氧化铜生成铜和二氧化碳,二氧化碳与石灰水反应生成碳酸钙和水;②由于氢气还原氧化铜生成了铜和水,浓硫酸具有吸水性,浓硫酸质量的增加量就是生成水的质量.③在A装置前放一除水装置(例如用浓硫酸).
故答案为:(1)相同温度;间歇通入氧气;(2)①石灰水变浑浊,A中黑色粉末变为红色;CO+CuO
 Cu+CO2;CO2+Ca(OH)2=CaCO3↓+H2O②称量反应前后装置B的质量并进行比较③在装置A前增加除水分装置.
Cu+CO2;CO2+Ca(OH)2=CaCO3↓+H2O②称量反应前后装置B的质量并进行比较③在装置A前增加除水分装置.点评:通过回答本题知道了验证燃烧条件的对照实验的设计方法,掌握了氢气和一氧化碳的验证方法.

练习册系列答案
相关题目
(2010?绵阳)欲除去物质中所含少许杂质,所用的方法错误 的是( )
|
(2010?绵阳)质量分数不同的硫酸溶液其密度不相同,对照表如下:
将10mL98%浓硫酸中加水稀释至100ml,取10mL该稀硫酸与足量锌反应制取氢气,请按要求完成系列问题的解答(计算结果保留一位小数):
(1)10mL98%的浓硫酸中含gH2SO4.
(2)列式计算消耗金属锌的质量.
(3)分析表中数据,可以归纳出硫酸溶液的质量分数与密度的关系是.10mL水和10mL质量分数为b%的硫酸溶液混合,混合后溶液的质量分数应该在至之间.
| 质量分数 | 10% | 20% | 30% | 40% | 50% | 60% | 70% | 80% | 90% | 98% |
| 密度(g/mL) | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.81 | 1.84 |
(1)10mL98%的浓硫酸中含gH2SO4.
(2)列式计算消耗金属锌的质量.
(3)分析表中数据,可以归纳出硫酸溶液的质量分数与密度的关系是.10mL水和10mL质量分数为b%的硫酸溶液混合,混合后溶液的质量分数应该在至之间.