题目内容
水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要关心水、爱护水、节约用水.(1)我国规定生活饮用水的水质必须达到下述四项指标:a.不得呈现异色 b.不得有异味 c.应澄清透明 d.不得含有细菌和病毒.其中“c指标”可以通过
(2)生活中可以采用
(3)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如下图所示.
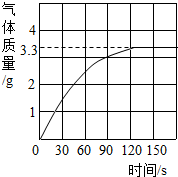
①从图中可以看出,12.5g水垢与盐酸反应后生成的二氧化碳最多是
②水垢中碳酸钙的质量分数是多少?
分析:(1)活性炭具有吸附作用,可以吸附色素和异味;过滤可以除去水中的不溶性杂质;消毒可以杀死水中的病毒和细菌.
(2)用肥皂水可以检验硬水和软水,生活中常用煮沸的方法将硬水软化.
(3)由图示可知,反应最终产生的二氧化碳的质量为3.3g,再根据碳酸钙与盐酸反应的化学方程式可以求出水垢中碳酸钙的质量,进而求出水垢中碳酸钙的质量分数.
(2)用肥皂水可以检验硬水和软水,生活中常用煮沸的方法将硬水软化.
(3)由图示可知,反应最终产生的二氧化碳的质量为3.3g,再根据碳酸钙与盐酸反应的化学方程式可以求出水垢中碳酸钙的质量,进而求出水垢中碳酸钙的质量分数.
解答:解:(1)过滤可以除去水中的不溶性杂质.故答案为:过滤;
(2)用肥皂水可以检验硬水和软水,生活中常用煮沸的方法将硬水软化.故答案为:肥皂水;煮沸;
(3)①由图中曲线可以看出,当生成的气体质量为3.3g时,随着时间的推移,二氧化碳的质量不再改变,说明反应停止.故答案为:3.3g;
②解:设反应掉的碳酸钙质量为x,
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
x 3.3g
=
x=7.5g
x100%=60%
答:水垢中碳酸钙的质量分数是60%.
(2)用肥皂水可以检验硬水和软水,生活中常用煮沸的方法将硬水软化.故答案为:肥皂水;煮沸;
(3)①由图中曲线可以看出,当生成的气体质量为3.3g时,随着时间的推移,二氧化碳的质量不再改变,说明反应停止.故答案为:3.3g;
②解:设反应掉的碳酸钙质量为x,
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
x 3.3g
| 100 |
| 44 |
| x |
| 3.3g |
x=7.5g
| 7.5g |
| 12.5g |
答:水垢中碳酸钙的质量分数是60%.
点评:本题考查水的净化方法,并要求能从图象中找出有效数据进行化学方程式的计算.

练习册系列答案
相关题目
 水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要关心水、爱护水、节约用水.
水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要关心水、爱护水、节约用水.
