题目内容
【题目】化学兴趣小组的同学欲测定实验室中某黄铜(铜锌合金)样品中铜的质量分数(不考虑黄铜中的其他杂质,请你参与他们的探究过程。称量10 g粉末状黄铜样品放入烧杯中,量取45 mL稀盐酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
第一次 | 第二次 | 第三次 | |
加入稀盐酸的体积(mL) | 15 | 15 | 15 |
生成氢气的质量(g) | 0.04 | m | 0.02 |
试求:
(1)求m的数值。m=_________
(2)求此黄铜样品中铜的质量分数________。
【答案】 0.04 67.5%。
【解析】(1)根据表格可以发现,第一次加入15mL盐酸生成0.04g氢气,第三次加入15mL盐酸还能生成并且只生成0.02g氢气,说明直到第三次反应才结束,并且盐酸有剩余;同时说明第二次加入15mL盐酸时完全反应,生成氢气的质量可按照第一次的数量关系(15ml对应0.04g)类推,而得出m为0.04g;(2)根据表格可知,共生成氢气的质量为0.04g+0.04g+0.02g=0.1g,设需要锌的质量为x,则:
Zn+2HCl=ZnCl2+H2↑
65 2
x 0.1g
![]()
x=3.25g
所以此黄铜样品中铜的质量分数为:![]() ×100%=67.5%;
×100%=67.5%;
答:此黄铜样品中铜的质量分数是67.5%。

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案【题目】高氯酸钾( KClO4) 可用作火箭推进剂,其溶解度如下表。下列说法不正确的是
温度/℃ | 20 | 40 | 60 | 80 |
溶解度/g | 1.68 | 3.73 | 7.3 | 13.4 |
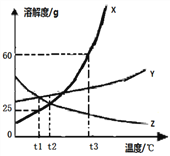
A. 高氯酸钾的溶解度随温度降低而减小
B. 80℃的高氯酸钾饱和溶液冷却至40℃一定有晶体析出
C. 60℃时,高氯酸钾饱和溶液中溶质的质量分数小于7.3%
D. 20℃时,向2 g高氯酸钾中加入98 g水,所得溶液的溶质质量分数为2%
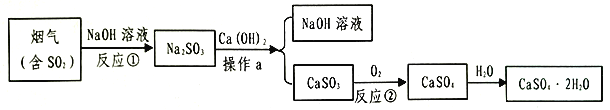
【题目】自来水消毒过程中常发生下列转化:
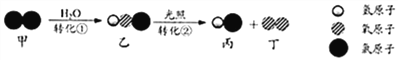
下列说法正确的是 ( )
A. 反应前后分子不可分 B. 转化①是化合反应
C. 转化②中丙和丁的分子个数之比为1︰1 D. 转化①、②中氯元素的化合价都发生变化
【题目】下列四个图像反映了对应实验过程中相关量的变化,其中错误的是
|
|
|
|
A.部分变质的NaOH溶液中滴加稀盐酸 | B.HCl气体的溶解度受温度影响的变化曲线 | C.等质量的Mg粉和Fe粉与足量相同浓度的稀盐酸反应 | D.硫酸溶液稀释过程中pH的变化曲线 |
A. A B. B C. C D. D