题目内容
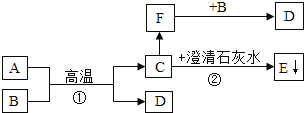
【题目】根据如图回答问题。
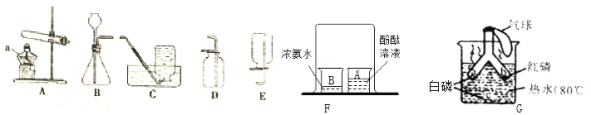
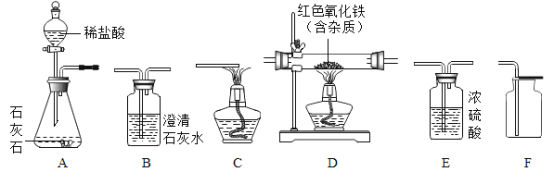
(1)仪器a的名称是______。
(2)用高锰酸钾制取氧气的化学方程式为______,用C装置收集的气体应具有的性质是______。
(3)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是______,用D装置收集二氧化碳的验满方法是______。
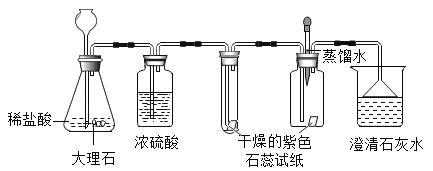
(4)实验F中观察到的实验现象是______,实验结论是______。
(5)实验G中观察到的实验现象是______,化学方程式为______。
【答案】酒精灯 2KMnO4![]() K2MnO4+MnO2+O2↑ 不溶于水且不与水反应 B 将燃着的木条接近集气瓶口,若熄灭则收集满 酚酞试液变红 氨分子从烧杯A扩散到烧杯中B,溶于水使酚酞试液变红 a处白磷燃烧,b处红磷未燃烧,c处白磷未燃烧 4P+5O2
K2MnO4+MnO2+O2↑ 不溶于水且不与水反应 B 将燃着的木条接近集气瓶口,若熄灭则收集满 酚酞试液变红 氨分子从烧杯A扩散到烧杯中B,溶于水使酚酞试液变红 a处白磷燃烧,b处红磷未燃烧,c处白磷未燃烧 4P+5O2![]() 2P2O5
2P2O5
【解析】
(1)仪器a是酒精灯,是常用的加热仪器,故填酒精灯;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平,故填2KMnO4![]() K2MnO4+MnO2+O2↑;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,故填不溶于水且不与水反应;
K2MnO4+MnO2+O2↑;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,故填不溶于水且不与水反应;
(3)实验室制取CO2,是在常温下用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应不需要加热,发生装置故填B;二氧化碳的验满方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了,故填将燃着的木条接近集气瓶口,若熄灭则收集满;
(3)实验F中观察到的实验现象是酚酞试液变红,故填酚酞试液变红;出现该现象的原因是氨分子从烧杯B扩散到烧杯中A,溶于水使酚酞试液变红,故填氨分子从烧杯A扩散到烧杯B中,溶于水使酚酞试液变红;
(4)实验G中a处白磷燃烧而b处红磷不燃烧,说明白磷的着火点比红磷的低;a处白磷燃烧而c处白磷不燃烧,二者温度均达到了着火点,但是热水中的白磷没有与氧气接触,这说明燃烧需要与氧气接触,故填a处白磷燃烧,b处红磷未燃烧,c处白磷未燃烧;磷燃烧生成五氧化二磷,反应的化学方程式故填4P+5O2![]() 2P2O5。
2P2O5。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】为了探究金属活动性,同学们将锌和铜分别放入稀硫酸中,锌的表面有气泡产生而铜不反应,写出锌和稀硫酸反应的化学方程式:_____。
老师告诉同学,铜和浓硫酸在加热的条件下也能反应且产生气体。
(提出问题)铜与浓硫酸反应的生成物是什么?其中气体是什么?
(猜想假设)同学们对产生的气体作出了猜想。
猜想一:氢气;
猜想二:二氧化硫;
猜想三:氢气和二氧化硫的混合气体。
同学们作出以上猜想的依据是_____。
(査阅资料)(1)二氧化硫有刺激性气味,会污染空气;
(2)二氧化硫可以使品红溶液褪色,能被氢氧化钾溶液吸收;
(3)浓硫酸具有吸水性,可以干燥气体。
(实验探究)师生设计了如下装置进行实验(部分仪器省略),请完成下列表格。
主要实验步骤 | 主要现象 | 解释或结论 |
①加热装置A一段时间 | 装置B中的现象是_____ | 有二氧化硫生成 |
②点燃装置D处酒精灯 | 装置D玻璃管中无明显现象 | 猜想_____正确 |
③停止加热,将铜丝上提,向装置A中玻璃管鼓入空气 | ||
④冷却,观察A中溶液颜色 | A中液体变为_____色 | 有硫酸铜生成 |
(表达交流)
(1)在步骤③中,鼓入空气的目的是_____。
(2)铜与浓硫酸反应的化学方程式为:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+_____。
CuSO4+SO2↑+_____。
(反思拓展)
若将装置A中铜丝换成锌片,随着反应的进行,硫酸的浓度逐渐变小,装置D玻璃管中看到的现象是_____。