题目内容
【题目】向盛有少量硝酸镁溶液的烧杯中滴加氢氧化钾溶液至恰好反应。请回答:
(1)上述反应中的实验现象为____________________。
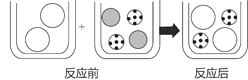
(2)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子(填离子符号)。
![]() ______;
______;![]() ______;
______;![]() ____。
____。
(3)在硝酸镁溶液中滴加__________溶液,也会出现上述实验中相同的实验现象,从微观角度分析,产生该现象的原因是______________________________。
【答案】有白色沉淀生成 NO3- OH- K+ 氢氧化钠 镁离子能与氢氧根离子结合生成氢氧化镁沉淀
【解析】
(1)硝酸镁溶液与氢氧化钾溶液反应生成氢氧化镁白色沉淀和硝酸钾,反应中的实验现象为有白色沉淀生成;
(2)硝酸镁溶液与氢氧化钾溶液反应生成氢氧化镁白色沉淀和硝酸钾,反应后氢氧化镁沉淀析出,溶液中含有的离子是硝酸根离子和钾离子,因此![]() 表示K+,
表示K+,![]() 表示NO3-,反应后
表示NO3-,反应后![]() 消失,是因为和氢氧根离子结合生成了氢氧化镁沉淀,因此
消失,是因为和氢氧根离子结合生成了氢氧化镁沉淀,因此![]() 表示OH-;
表示OH-;
(3)在硝酸镁溶液中滴加氢氧化钠溶液,也会出现上述实验中相同的实验现象,从微观角度分析,产生该现象的原因是镁离子能与氢氧根离子结合生成氢氧化镁沉淀。

练习册系列答案
相关题目