题目内容
【题目】碘元素具有预防和治疗甲状腺肿的作用,人体缺碘时易患粗脖子病。为了消除碘缺乏病,我国政府规定居民的食用盐必须是加碘食盐,简称碘盐。所谓碘盐就是在食盐中加入一定量的碘酸钾。下表为某精制碘盐包装袋上的部分文字说明:
配料表 | 食用盐、碘酸钾 |
含碘量 | (20mg--40mg)/Kg |
保质期 | 18个月 |
食用方法 | 待食物烹调好后在放碘盐,勿长时间炖炒 |
贮藏指南 | 避热、避光、密封、防潮 |
(1)已知碘酸钾的化学式为KIO3。
①碘酸钾中碘元素的化合价为__________;②碘酸钾的相对分子质量为____________。
③一定量的碘酸钾中含有12.7g碘,则碘酸钾的质量为_________g。
(2)由食用方法和贮藏指南,可推测碘酸钾的化学性质之一是_______________________________。
(3)若1000g碘盐中约含20mg碘。
①这里标明的碘的含量是指___________;
A.碘单质 B.碘元素 C.碘原子 D.碘分子
②若成人每天摄入5g这样的“碘盐”,至少补充碘元素_____mg(写出计算过程)。
【答案】 +5 214 21.4 受热易分解(或受热不稳定)(合理即给分) B 由含碘量(20--40)mg/kg可知,成人每天摄入5g这样的“碘盐”,至少补充碘元素质量为:5g×20mg/1000g=0.1mg
【解析】【试题分析】本题利用碘酸钾为知识情境考查了化合价,根据化学式计算等。解题要利用化合物中元素的化合价和代数和为零以及化学式意义。
(1)①钾元素的化合价为+1价,氧元素的化合价为﹣2价,设碘元素的化合价为X,则碘元素的化合价为:(+1)+X+(﹣2)×3═0 X═+5;
②碘酸钾(KIO3)的相对分子质量=39+127+16×3=214;
③需要碘酸钾的质量=12.7g÷![]() =21.4g;
=21.4g;
(2)碘酸钾的食用方法是:待食物烹调好后再放入碘盐,储存方法是密封、避光、防潮湿.说明碘酸钾不能接触较高的温度,因此说明碘酸钾具有受热易分解的性质;
(3)①加碘盐中的碘指的是碘元素,故选B;
②1000g碘盐中约含20mg碘。成人每天摄入5g这样的“碘盐”,至少补充碘元素质量为:5g×20mg/1000g=0.1mg

【题目】某小组对H2O2溶液制取氧气进行了如下探究:
【探究一】:探究不同催化剂对H2O2分解快慢的影响
该小组采用了如下图所示装置进行实验,实验中催化剂均为0.4g,H2O2溶液浓度均为10%20mL,在C框中连接导管和量筒,并测量收集到50mL水时的某项数据,经计算后的数据如下表:

催化剂种类 | 气体产生速率(mL/s) |
二氧化锰 | 3.5 |
氧化铜 | 4.5 |
活性炭 | 5.8 |
(1)检查A装置气密性的方法是:用弹簧夹夹住A装置右侧导气管,打开①的两个活塞,向其中加水,若___________,则气密性良好。
(2)C框内选用C1或C2装置,对该探究实验结论有无影响______。
(3)从实验数据可知:相同条件下表中催化剂的催化效果由强到弱依次为________。
(4)该探究实验中,需要测定的数据是____________。
(5)当量筒中收集到50mL水时,双氧水分解出的氧气体积______50mL(填“大于”、“等于”、“小于”)。
【探究二】:探究H2O2溶液浓度对分解速率的影响
如图:在250mL三颈瓶中,加入MnO2均为0.5g,在恒压漏斗中加入不同浓度的H2O2溶液各20mL分别进行实验。并用温度传感器测量并绘制出瓶内温度与时间关系图。如下图所示。
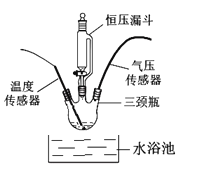
再将该装置的三颈瓶浸入水浴池中(该池可使瓶内的溶液温度恒定在20℃),用上述实验中相同量的各物质重复上述实
验,用气压传感器测量并绘制出瓶内气压与时间关系图。如下图所示。
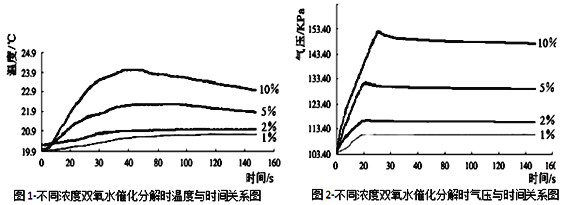
(6)实验中,恒压漏斗的作用是__________。
(7)由图1知道:H2O2溶液分解时会_________热量(填“放出”或“吸收”)。
(8)由图2知道: H2O2溶液浓度越高,其分解反应速率越______(填“快”或“慢”),以10%H2O2溶液为例,20S后三颈瓶内气压约由高缓慢降低的原因是_________。
(9)影响H2O2溶液分解速率的因素,除了催化剂的种类、H2O2溶液浓度外,还可能有的因素如:__________(请写出一种)。