题目内容
【题目】南海海域是我国固有领土,蕴藏着丰富的海洋资源。充分利用南海海洋资源,结合我国制碱工业先驱侯德榜发明的“侯氏制碱法”基本原理,模拟实现工业联合制取纯碱的过程如下(某些反应产物已略去):
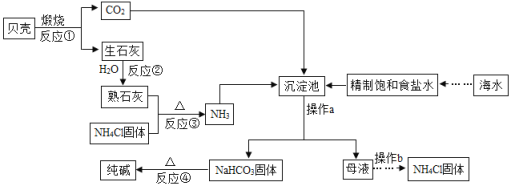
请回答下列问题:
(1)操作a的名称是________;
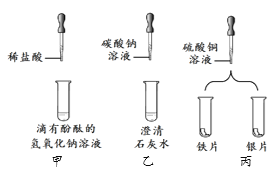
(2)下列物质中均能与贝壳主要成分、生石灰、熟石灰发生反应的是________(填字母)。
A 水 B 盐酸 C 二氧化碳
(3)沉淀池中发生的反应是:NaCl+H2O+NH3+CO2══NaHCO3↓+NH4Cl。通常情况下,1L水能溶解约1L二氧化碳或700L氨气。现向精制饱和食盐水中通入两种气体的顺序是:先通氨气形成饱和氨盐水,然后在加压条件下通入二氧化碳。这样操作的目的是____________。
(4)已知:固体![]() ,Ca(HCO3)2和NaHCO3化学性质相似。写出反应④的化学方程式:___________;请列举小苏打在生活中的一种常见用途_________。
,Ca(HCO3)2和NaHCO3化学性质相似。写出反应④的化学方程式:___________;请列举小苏打在生活中的一种常见用途_________。
(5)仔细观察流程图,其中可循环利用的物质除二氧化碳之外,还有_________。
(6)联合制碱法生产的纯碱(Ⅲ类)国家质量主要标准如下表所示:
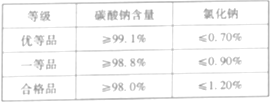
化学兴趣小组的同学设计并完成了如下实验来判断纯碱样品的等级(不考虑其他杂质参加反应)。称取10. 8g联合制碱法生产的纯碱样品,加入足量的水溶解,再加入足量的氯化钡溶液充分反应后过滤,将滤渣洗涤、干燥,得到碳酸钡固体19.7 g;另称取60 g联合制碱法生产的纯碱样品,加入足量的水溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后过滤,将滤渣洗涤、干燥,得到氯化银固体1.435 g。
①该纯碱样品中碳酸钠的质量分数为___________(计算结果精确到0.01%)
②列式计算该纯碱样品中所含氯化钠的质量分数______(计算结果精确到0.01%)
③该纯碱样品的等级为________。
【答案】过滤 B 使溶液呈现碱性,从而吸收更多的二氧化碳,加速生成更多的碳酸氢钠 ![]() 治疗胃酸过多等 氯化铵 98.15% 0.98% 合格
治疗胃酸过多等 氯化铵 98.15% 0.98% 合格
【解析】
(1)操作a得到了固体和母液即实现了固体和液体的分离,为过滤;
(2)由于贝壳成分为碳酸钙,生石灰为氧化钙,而熟石灰是氢氧化钙,所以给出物质中能与贝壳主要成分、生石灰、熟石灰发生反应的是盐酸,水、二氧化碳不和碳酸钙反应。故选B。
(3)通常情况下,1L水能溶解约1L二氧化碳或700L氨气,即水直接溶解和吸收二氧化碳的能力很弱,所以先通氨气形成饱和氨盐水,让溶液呈现碱性,然后在加压条件下通入二氧化碳。这样操作的目的是使溶液呈现碱性,从而吸收更多的二氧化碳,加速生成更多的碳酸氢钠。
(4)![]() ,Ca(HCO3)2和NaHCO3化学性质相似,把对应钙元素的地方换上钠元素,结合化合价书写对应化学式,进而完成化学方程式为:
,Ca(HCO3)2和NaHCO3化学性质相似,把对应钙元素的地方换上钠元素,结合化合价书写对应化学式,进而完成化学方程式为:![]() ;碳酸氢钠可以和盐酸反应,所以小苏打在生活中的一种常见用途治疗胃酸过多等。
;碳酸氢钠可以和盐酸反应,所以小苏打在生活中的一种常见用途治疗胃酸过多等。
(5)在流程图中二氧化碳和氯化铵开始是反应物,后来是生成物,所以在过程中可循环利用。
(6)称取10.8g联合制碱法生产的纯碱样品,加入足量的水溶解,再加入足量的氯化钡溶液充分反应后过滤,将滤渣洗涤、干燥,得到碳酸钡固体19.7 g;
设该纯碱样品中碳酸钠的质量分数为x
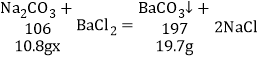
![]()
x≈98.15%>98.0%
取60 g联合制碱法生产的纯碱样品,加入足量的水溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后过滤,将滤渣洗涤、干燥,得到氯化银固体1.435 g。
设该纯碱样品中所含氯化钠的质量分数为y
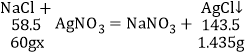
![]()
y≈0.98%<1.20%
该纯碱样品的等级为合格。

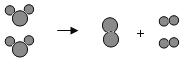
【题目】甲、乙、丙三种物质的转化关系如图所示(“→”表示反应一步实现,部分物质和反应条件已略去)。下列选项不能实现图示转化的是
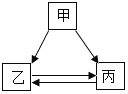
选项 | 甲 | 乙 | 丙 |
A | H2O2 | O2 | H2O |
B | KOH | KCl | KNO3 |
C | C | CO2 | CO |
D | CuO | Cu | Cu(NO3)2 |
A. AB. BC. CD. D