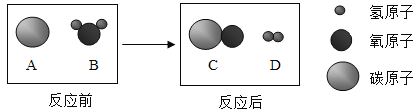
题目内容
【题目】我国医学著作博大精深,许多化学物质很早就出现在了我国医书中。如李时珍的《本草纲目》中就有绿矾(FeSO4﹒7H2O)的相关记载。绿矾又名皂矾、青矾,性酸、凉、无毒,主要药用功能是除湿、解毒、收敛、止血。
(1)写出铁与稀硫酸反应的化学方程式:________________。
(2)某实验小组欲用久置的硫酸亚铁溶液制备绿矾(FeSO4﹒7H2O)晶体,小明同学提出该硫酸亚铁溶液可能变质了,于是进行了以下探究活动:
(查阅资料)
①FeSO4易被空气中的氧气氧化成Fe2 (SO4)3而变质。
②Fe2+能使紫色酸性高锰酸钾溶液褪色。
③Fe3+的检验:向含Fe3+的溶液中滴加无色的KSCN(硫氰化钾)溶液,溶液会变为血红色。
(猜想与假设)猜想1:该硫酸亚铁溶液没有变质;
猜想2:该硫酸亚铁溶液部分变质;
猜想3:________________。
(设计实验并验证)
实验操作步骤 | 实验现象 | 实验结论 |
取少量样品于试管中,加人3~4滴___________溶液 | 试管中溶液_______ | 猜想2成立 |
取少量样品于试管中,加入3~4滴酸性高锰酸钾溶液 | ___________________ |
(实验拓展)该实验小组继续查阅资料得知,单质铁能与硫酸铁溶液反应生成硫酸亚铁。写出上述反应的化学方程式:____________。实验室配制硫酸亚铁溶液时,为了防止FeSO4被空气氧化,可以向溶液中加入适量的固体物质是_________________。
【答案】![]() 该硫酸亚铁溶液全部变质 KSCN(或硫氰化钾) 变成血红色 紫色酸性高锰酸钾溶液褪色
该硫酸亚铁溶液全部变质 KSCN(或硫氰化钾) 变成血红色 紫色酸性高锰酸钾溶液褪色 ![]() 铁粉
铁粉
【解析】
(1)铁与稀硫酸反应生成硫酸化亚铁和氢气,反应的化学方程式: ![]() 。
。
(2)某实验小组欲用久置的硫酸亚铁溶液制备绿矾(FeSO4﹒7H2O)晶体,小明同学提出该硫酸亚铁溶液可能变质了,于是进行了以下探究活动:
猜想与假设:
根据“猜想1:该硫酸亚铁溶液没有变质”、“猜想2:该硫酸亚铁溶液部分变质”,猜想3为: 该硫酸亚铁溶液全部变质。
设计实验并验证:
含Fe3+的溶液中滴加无色的KSCN(硫氰化钾)溶液,溶液会变为血红色,取少量样品于试管中,加人3~4滴KSCN(或硫氰化钾)溶液,试管中溶液变成血红色,说明该硫酸亚铁溶液部分变质;Fe2+能使紫色酸性高锰酸钾溶液褪色,取少量样品于试管中,加入3~4滴酸性高锰酸钾溶液,紫色酸性高锰酸钾溶液褪色,说明该硫酸亚铁溶液部分变质;故有:
实验操作步骤 | 实验现象 | 实验结论 |
取少量样品于试管中,加人3~4滴KSCN(硫氰化钾)溶液 | 试管中溶液变成血红色 | 猜想2成立 |
取少量样品于试管中,加入3~4滴酸性高锰酸钾溶液 | 紫色酸性高锰酸钾溶液褪色 |
实验拓展:
单质铁能与硫酸铁溶液反应生成硫酸亚铁,反应的化学方程式: ![]() ,因此实验室配制硫酸亚铁溶液时,为了防止FeSO4被空气氧化,可以向溶液中加入适量的固体物质是铁粉。
,因此实验室配制硫酸亚铁溶液时,为了防止FeSO4被空气氧化,可以向溶液中加入适量的固体物质是铁粉。

【题目】某兴趣小组的同学将一定质量的碳酸氢钠和稀硫酸混合,充分反应,有气泡逸出。同学们对反应后溶液中溶质的成分进行了探究。
(猜想与假设)
猜想①:溶质成分是 _______________
猜想②:溶质成分是硫酸钠、碳酸氢钠
猜想③:溶质成分是硫酸钠、硫酸
(查阅资料)NaHCO3溶液呈碱性。
(实验药品)pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
(实验探究)同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成下表。
实验方案 | A | B | C | D |
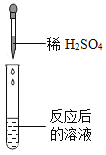
实验操作 |
|
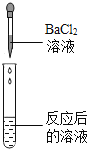
|
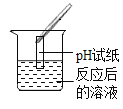
|
|
实验现象 | _______ | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH<7 | __________ |
(得出结论)猜想③正确。
(评价反思)
(1)写出碳酸氢钠和稀硫酸反应的化学方程式_____________。
(2)上述实验中存在一处明显错误操作的是方案_______________(填字母序号)。
(3)有同学认为仅凭B实验方案中的实验现象,不能得出“猜想③”正确,其理由是 ____________。
(4)用上述药品,请你再设计一个不同的实验方案证明“猜想③”正确_______________。