题目内容
有NaCl和Na2CO3混合物13.6g,与90.8g盐酸恰好完全反应,共放出4.4g气体.求:
(1)原混合物中Na2CO3的质量.(2)反应后所得溶液的溶质质量分数.
(1)原混合物中Na2CO3的质量.(2)反应后所得溶液的溶质质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)碳酸钠与盐酸反应放出二氧化碳而氯化钠不与盐酸反应,根据反应的化学方程式,由生成二氧化碳的质量可计算样品中碳酸钠的质量;
(2)反应后所得溶液为氯化钠溶液,其中氯化钠由原样品中氯化钠和反应生成氯化钠两部分所组成;由生成二氧化碳质量可计算出生成的氯化钠的质量,样品质量与碳酸钠质量差则为样品中氯化钠的质量,据此分析解答;
(2)反应后所得溶液为氯化钠溶液,其中氯化钠由原样品中氯化钠和反应生成氯化钠两部分所组成;由生成二氧化碳质量可计算出生成的氯化钠的质量,样品质量与碳酸钠质量差则为样品中氯化钠的质量,据此分析解答;
解答:解:(1)设样品中碳酸钠的质量为x,生成氯化钠的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
=
=
x=10.6g; y=11.7g
(2)原固体中氯化钠的质量为13.6g-10.6g=3g,
反应后所得溶液的溶质质量分数=
×100%=14.7%;
答:(1)原混合物中Na2CO3的质量是3g;(2)反应后所得溶液中含溶质的质量分数为14.7%;
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
| 106 |
| x |
| 44 |
| 4.4g |
| 117 |
| y |
| 44 |
| 4.4g |
x=10.6g; y=11.7g
(2)原固体中氯化钠的质量为13.6g-10.6g=3g,
反应后所得溶液的溶质质量分数=
| 11.7g+3g |
| 13.6g+90.8g-4.4g |
答:(1)原混合物中Na2CO3的质量是3g;(2)反应后所得溶液中含溶质的质量分数为14.7%;
点评:根据化学方程式可以表示反应中各物质的质量比,由反应中任意物质的质量可计算出反应中其它物质的质量.

练习册系列答案
相关题目

 碳酸钙可用于预防和治疗钙缺乏症.某实验小组同学要测定一种钙片中碳酸钙的含量.
碳酸钙可用于预防和治疗钙缺乏症.某实验小组同学要测定一种钙片中碳酸钙的含量.
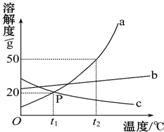 如图是a、b、c三种物质的溶解度曲线a与c的溶解度曲线相交于P点.据图回答:(1)P点的含义是
如图是a、b、c三种物质的溶解度曲线a与c的溶解度曲线相交于P点.据图回答:(1)P点的含义是