题目内容
【题目】如图是某兴趣小组探究空气中氧气的体积分数的实验,回答下列问题:
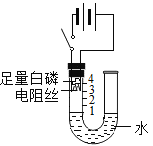
(1)电阻丝在实验中的作用是_____;
(2)加足量白磷的目的是_____;其燃烧的化学方程式为_____。
(3)装置冷却到室温,可观察到的现象是_____,据此得出空气中氧气的体积分数约为20%的结论。
【答案】.加热,使温度达到白磷的着火点 将容器内空气中的氧气消耗完全,使结果更准确; 4P+5O2![]() 2P2O5 U型管左侧液面约上升到刻度1处
2P2O5 U型管左侧液面约上升到刻度1处
【解析】
磷在氧气中点燃生成五氧化二磷。
(1)电阻丝在实验中的作用是加热,使温度达到白磷的着火点。
(2)加足量白磷的目的是将容器内空气中的氧气消耗完全,使结果更准确;磷在氧气中点燃生成五氧化二磷,其燃烧的化学方程式为4P+5O2![]() 2P2O5。
2P2O5。
(3)磷在氧气中点燃生成五氧化二磷,消耗了装置中的氧气,装置冷却到室温,可观察到的现象是U型管左侧液面约上升到刻度1处,据此得出空气中氧气的体积分数约为20%的结论。

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
【题目】下面是同学们测定黄铜(铜锌合金)中铜的质量分数的过程。
(1)小华同学取10 g黄铜,加入足量的稀硫酸,共收集到气体0.2 g,则黄铜中铜的质量分数是多少__________?(写出计算过程)
(2)小婷同学另取10 g黄铜于烧杯中,将120 g稀硫酸分六次加入烧杯中,测得加入的稀硫酸质量和烧杯中剩余物的质量如下表,表中m=___________。
次数 | 一 | 二 | 三 | 四 | 五 | 六 |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量/g | 29.96 | 49.92 | m | 89.84 | 109.8 | 129.8 |