题目内容
【题目】2018年12月8日2时23分,中国在西昌卫星发射中心用长征三号乙运载火箭成功发射嫦娥四号探测器,开启了月球探测的新旅程。
(1)月球中含有丰富氦﹣3原子(其质子数为2,中子数为1),则该原子的核外电子数为____。
(2)在航天飞机和火箭上用到了稀罕的钪钛合金。钪(Sc)在元素周期表中的信息及原子结构示意图如图1所示。
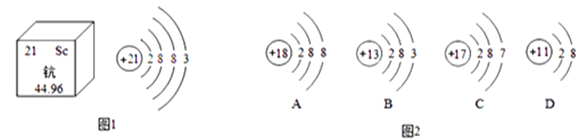
①钪属于_____(填“金属”或“非金属”)元素,其相对原子质量为_____。
②图2所表示的四种粒子中,与钪原子的化学性质相似的是_____。
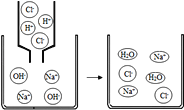
(3)很久之前运载火箭使用有毒的联氨(N2H4)和四氧化二氮作为火箭动力,下图是联氨和四氧化二氮反应的微观示意图,请写出其化学反应方程式_____。
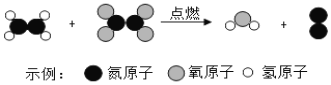
【答案】2 金属 44.96 B N2O4+2N2H4![]() 3N2+4H2O
3N2+4H2O
【解析】
由于在原子中质子数等于电子数,氦-3原子的质子数为2,则该原子的核外电子数为2。
(2)①钪的名称中带有“钅”字旁,属于金属元素,其相对原子质量为44.96。
②图2所表示的四种粒子中,B的最外层电子数与钪原子的最外层电子数相同,化学性质相似。
(4)由联氨和四氧化二氮反应的微观示意图可知,在点燃的条件下联氨和四氧化二氮反应生成了氮气和水,其化学反应方程式为:N2O4+2N2H4![]() 3N2+4H2O
3N2+4H2O
故答为:(1)2.(2)①金属,44.96;②B.(3)N2O4+2N2H4![]() 3N2+4H2O
3N2+4H2O

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【题目】在工业中硫酸铜有不少用途。某工厂用硫化铜(CuS)制硫酸铜,拟选择两个方案。
方案 | 方案① | 方案② |
原理 | CuS是在硫杆菌(催化剂)的作用下与空气中的氧气发生化合反应生成硫酸铜 | 2CuS+3O2 CuO+H2SO4=CuSO4+H2O |
(1)请写出方案①反应的化学方程式_____。
(2)在两个方案中①更合理。理由是方案①具有以下优点:
优点一:_____优点二:_____。
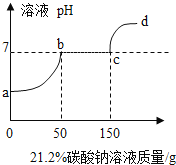
【题目】为了探究石灰石的纯度(假设样品中的杂质既不溶于水也不与盐酸反应),兴趣小组进行如下实验:先称取40g石灰石样品均分为4等份分别加入到四个烧杯中,然后再分别加入一定质量的相同浓度的盐酸,实验数据如表所示:
实验编号 | ① | ② | ③ | ④ |
稀盐酸的质量/g | 25 | 50 | 75 | 100 |
剩余固体的质量/g | 7.5 | 5 | 3 | 3 |
(1)石灰石的纯度是_____;
(2)计算所用稀盐酸的溶质质量分数_____(写出计算过程);
(3)实验④所得溶液中溶质的成分是_____(填写化学式)。
【题目】(1)实验是科学探究的重要手段,请按要求填写如表。
实验内容 | 蒸发结晶 | 稀释浓硫酸 |
实验操作 |
|
|
问题讨论 | ①当蒸发皿中出现_____时,停止加热。 | ②烧杯中物质A的名称是_____。 |
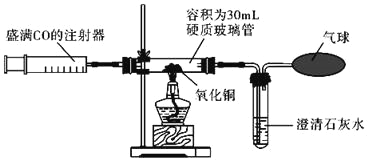
(2)如图是实验室制取和收集气体的装置,请按要求回答下列问题。
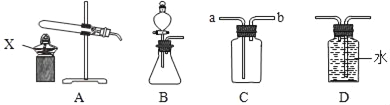
①仪器X的名称是_____。
②实验室用高锰酸钾制取并收集较纯净的氧气,应选用的发生装置和收集装置的组合是_____(填字母),该反应的化学方程式是_____。
③实验室收集CO2时,选用C装置而不选用D装置的理由是_____,CO2气体应从C装置的_____处(填“a”或“b”)进入。