题目内容
【题目】某实验小组根据下图所示装置(图中固定装置省略)探究燃烧的条件和酸、碱、盐的性质,其中装置甲的试管中盛有固体粉末B,分液漏斗中盛有足量溶液A,装置乙中盛有足量液体。请回答问题:
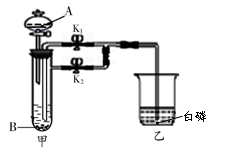
(1)关闭K1,打开K2,若装置乙中水下有少量白磷(此时水温35℃),实验时将足量A(H2O2溶液)滴加到B(MnO2)中后,关闭分液漏斗活塞,则乙中有气泡冒出,白磷不燃烧,说明燃烧还需要 ;若迅速关闭K2,待反应一段时间后打开K1,可能出现的现象是 ,且白磷燃烧。
(2)关闭K1,打开K2,装置乙中有石灰水。实验时将A(盐酸)滴加到B(白色固体)中后,关闭分液漏斗活塞,看到乙的溶液中有气泡冒出,变浑浊,那么乙中反应的化学方程式是 ;当甲中不再产生气泡后,在不改变装置的情况下,进行以下操作 ,能使乙中液体流入甲中。
【答案】(1)达到可燃物着火点;甲中液体流入乙;
(2)CO2+Ca(OH)2=CaCO3↓+H2O; 关闭K1,向A中加入氢氧化钠浓溶液,将其滴入甲中,打开K1或K2
【解析】
试题分析:则乙中有气泡冒出,说明产生氧气,但白磷不燃烧,说明燃烧还需要达到可燃物着火点;看到乙的溶液中有气泡冒出,变浑浊,说明产生的气体是二氧化碳,溶液是氢氧化钙;当甲中不再产生气泡后,在不改变装置的情况下,进行以下操作关闭K1,向A中加入氢氧化钠浓溶液,将其滴入甲中,打开K1或K2。

练习册系列答案
相关题目