题目内容
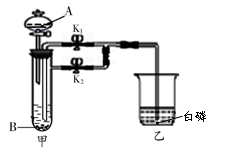
【题目】(5分)某实验小组利用下图所示装置进行研究CO2性质和燃烧条件的实验。

(1)研究CO2与水反应:进行此实验时,将C装置a、b两端分别与B、D装置连接A中液体为紫色石蕊溶液,B中固体为碳酸钠,C中液体为浓硫酸,D中放一朵干燥的紫色石蕊小花。将分液漏斗中的稀硫酸滴入B中。A中发生反应的化学方程式为 ;观察到 ,说明使紫色石蕊变色的是碳酸、不是CO2。
(2)研究燃烧的条件:进行此实验时,将C装置b、a两端分别与B、 D装置连接A和C的液体底部靠近导管口分别固定一小块白磷,B中固体为二氧化锰。将分液漏斗中的液体滴入B中。B中发生反应的化学方程式为 ;A液体为冷水,C中液体为___;观察到 ,说明可燃物燃烧需要与氧气接触、温度达到着火点。
【答案】(1)H2O + CO2 === H2CO3 A中紫色石蕊溶液变红,D中干燥紫色小花不变色
(2)2H2O2 二氧化锰 2H2O + O2 ↑ 热水 A中白磷不燃烧,C中白磷在液面下时不燃烧,露出液面后开始燃烧
【解析】
试题分析:A中发生反应的化学方程式为H2O + CO2 === H2CO3;所以A中紫色石蕊溶液变红,D中干燥紫色小花不变色说明使紫色石蕊变色的是碳酸、不是CO2;漏斗内的药品是过氧化氢,目的是在二氧化锰催化的作用下产生氧气,让白磷和氧气接触发生燃烧。为了对比物质的燃烧需要达到都着火点,所以C中要放入热水。

练习册系列答案
相关题目