题目内容
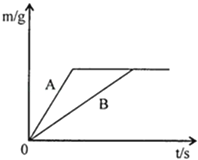
【题目】将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.
(1)写出锌与稀硫酸反应的化学方程式____.该反应的基本类型为___反应;
(2)对于该图象的理解,下列说法正确的是____(填序号).
①A表示锌和稀硫酸的反应曲线 ②反应结束后两种金属一定都有剩余
③反应结束后稀硫酸都没有剩余 ④反应结束后消耗两种金属的质量相等
⑤反应结束后所得溶液质量相等.
【答案】Zn+H2SO4═ZnSO4+H2↑ 置换 ①③
【解析】
(1)锌与硫酸反应生成硫酸锌和氢气,方程式是:Zn+H2SO4═ZnSO4+H2↑;该反应由一种单质和化合物反应生成另一种单质和化合物,符合置换反应的特点,属于置换反应;故答案为Zn+H2SO4═ZnSO4+H2↑;置换;
(2)由已知:“等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸充分反应”进行
①锌的活动性比铁的活动性强,所以等质量的金属,锌反应的时间短,正确;
②由图示可知:生成的氢气的质量相等,所以硫酸均反应完;Zn+H2SO4═ZnSO4+H2↑,Fe+H2SO4═FeSO4+H2↑,由方程式分析可知:如果锌恰好反应,则铁有剩余;故错误;
③置换反应是金属置换酸中的氢元素,所以若生成的氢气的质量相等,硫酸均反应完;故正确;
④根据化学方程式Fe+H2SO4═FeSO4+H2↑,可知每56g铁生成2g氢气,根据化学方程式Zn+H2SO4═ZnSO4+H2↑,可知每65g锌反应生成2g氢气;所以若是相等质量的铁和锌与硫酸反应,铁生成氢气多,而不会相等,故错误;
⑤因为溶液中的水都是一样多的,但是生成的硫酸铁和硫酸锌的质量相比硫酸锌的质量更重,故溶液质量不同,故错误;
故答案为①③.

 考前必练系列答案
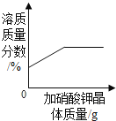
考前必练系列答案【题目】下列图象能正确反映其对应关系的是( )
A.某温度下,向一定量的硝酸钾不饱和溶液中不断加入硝酸钾晶体 |
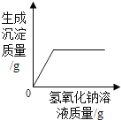
B.向稀盐酸和氯化铜的混合溶液中加入过量的氢氧化钠溶液 |
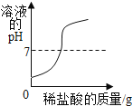
C.向氢氧化钠溶液中滴加过量的稀盐酸 |
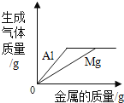
D.向盛有等质量、等溶质质量分数的稀硫酸的两支试管中,分别加入过量的金属镁和铝 |