题目内容
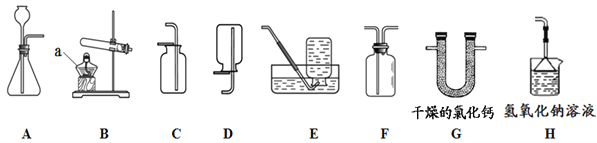
【题目】某同学设计了以下四个实验方案,理论上正确,操作上可行,经济上合理的是
A. ![]()
B. H2O![]() O2
O2![]() MgO
MgO
C. ![]()
D. MgCl2![]() Mg(OH)2
Mg(OH)2 ![]() Mg
Mg
【答案】A
【解析】根据金属活动性顺序,铜位于铁之后,反应在一般情况下就能进行分析解答;
B、工业上通常采取液化分离空气的方法获得氧气,而电解水的方便虽然可产生氧气,但反应需要消耗大量电解,不够经济;
C、根据铁和氧气在点燃的条件下生成四氧化三铁,而不能生成氧化铁;铁与水和氧气同时接触才能生成氧化铁分析解答;
D、氯化镁与氢氧化钠发生复分解反应生成氢氧化镁沉淀和氯化钠,氢氧化镁不能电解生成镁;工业上获得金属镁采取电解氯化镁的方法。
解:A、氧化铜一般情况下就能与稀盐酸反应生成氯化铜,而铁的活动性比铜强。能与氯化铜反应,置换出氯化铜里面的铜;故A确;
B、水通电分解可生成氧气,镁与氧气反应可以生成氧化镁,因此方案在理论上正确,但通过空气获得氧气要比电解水更经济,因此该方案在经济上不够合理;故B不正确;
C、铁和氧气在点燃的条件下生成四氧化三铁,而不能生成氧化铁;铁与水和氧气同时接触才能生成氧化铁,且反应需要的时间很长;故C正确;
D、氯化镁与氢氧化钠反应生成氢氧化镁沉淀,而氢氧化镁却不能分解生成金属单质镁,此方案理论上不正确;故D不正确;
故选A。

 名校课堂系列答案
名校课堂系列答案【题目】现有10%的Na2CO3溶液,请按下面要求计算:
(1)106 g上述溶液中所含溶质的质量 g。
(2)106 g上述溶液与足量10%的盐酸反应,最多可生成CO2多少克?
(3)向106 g上述溶液中逐滴加入10%的盐酸并不断搅拌,此时发生的反应为Na2CO3+HCl===NaHCO3+NaCl;当Na2CO3全部转化为NaHCO3后,再加入盐酸才开始放出CO2。请在图中画出产生气体的曲线。
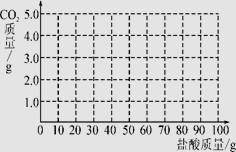
(4)另取10%的Na2CO3溶液边搅拌边加入10%的盐酸,有关反应物与生成物的量如下表:
物质 | Na2CO3 | HCl | X | NaCl | CO2 | H2O |
质量/g | 31.8 | 14.6 | 16.8 | 23.4 | 4.4 | w |
则w= ,
写出该反应的化学方程式 。
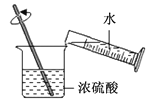
【题目】如下图所示进行实验,容器I、II体积相同,装置气密性良好,实验开始前红墨水左右两端液面相平。实验时同时将针筒内溶质质量分数相同且足量的稀硫酸全部迅速注入容器中,实验操作如下表:
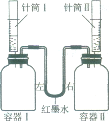
实验编号 | 容器Ⅰ | 针筒Ⅰ | 容器Ⅱ | 针筒Ⅱ |
甲 | 0.01mol镁 | 15mL稀硫酸 | 0.01mol 锌 | 15mL稀硫酸 |
乙 | 0.01mol锌 | 15mL稀硫酸 | 0.01mol铝 | 15mL稀硫酸 |
丙 | 0.01mol铜 | 15mL稀硫酸 | 0.01molg锌 | 15mL稀硫酸 |
实验结束红墨水左右两端液面呈现左高右低。能符合该实验现象的实验编号为
A. 甲、乙 B. 甲、丙
C. 乙、丙 D. 甲、乙、丙
【题目】某腐蚀印刷电路板的废液中含有CuCl2和FeCl2,为了分析该废液的组成,取1 000 g废液,设计如下实验方案进行探究:
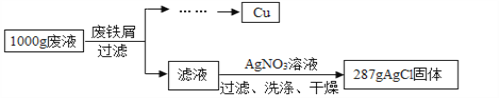
实验过程中加入废铁屑的质量、析出Cu的质量的数据记录如下表:
废铁屑的质量/g | 20 | 40 | 60 | 80 |
析出Cu的质量/g | 12.8 | 25.6 | 32 | 32 |
(注:废铁屑中的杂质不溶于废液也不与废液反应,不考虑过滤中的损失。)
(1)1 000 g废液与足量废铁屑完全反应,析出Cu的质量为_______ g。
(2)废铁屑中单质Fe的质量分数为_______________。
(3)计算1 000 g废液中CuCl2的质量分数_______。(写出计算过程,结果保留小数点后一位)
(4)1 000 g废液中FeCl2的质量分数为_________。(结果保留小数点后一位)