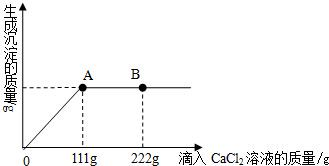
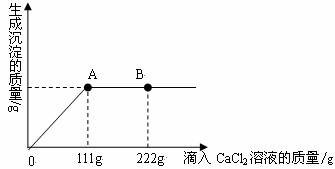
题目内容
学校探究小组为了测定市面销售的某品牌纯碱(杂质为NaCl)中碳酸钠的质量分数,进行了如下实验:
①在三个烧杯中都加入1lg样品及足量的水配成溶液;
②向三个烧杯加入质量不同的CaCl2粉末;(化学方程式为Na2CO3+CaCl2==CaCO3↓+2NaCl)
③将充分反应后生成的沉淀过滤、洗涤、干燥得到wg的白色同体。实验数据如下:
①在三个烧杯中都加入1lg样品及足量的水配成溶液;
②向三个烧杯加入质量不同的CaCl2粉末;(化学方程式为Na2CO3+CaCl2==CaCO3↓+2NaCl)
③将充分反应后生成的沉淀过滤、洗涤、干燥得到wg的白色同体。实验数据如下:
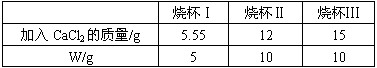
回答下列问题:
(1)碳酸钠中钠、碳、氧三种元素的质量比(最简比)为________。
(2)将烧杯Ⅲ的滤液蒸干,得到___g固体,该固体由_______和_______(只填化学式)组成。
(3)样品中碳酸钠的质量分数是多少?
(1)碳酸钠中钠、碳、氧三种元素的质量比(最简比)为________。
(2)将烧杯Ⅲ的滤液蒸干,得到___g固体,该固体由_______和_______(只填化学式)组成。
(3)样品中碳酸钠的质量分数是多少?
(1)23:6:24
(2)16;NaCl;CaCl2
(3)从实验数据可以看出烧杯III中的Na2CO3反应完全,故用烧杯III的数据计算
解:设样品中碳酸钠的质量为x。
Na2CO3+CaCl2==CaCO3↓+2NaCl
106 100
x 10g
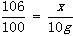 ,x=10.6g
,x=10.6g
碳酸钠的质量分数=
(2)16;NaCl;CaCl2
(3)从实验数据可以看出烧杯III中的Na2CO3反应完全,故用烧杯III的数据计算
解:设样品中碳酸钠的质量为x。
Na2CO3+CaCl2==CaCO3↓+2NaCl
106 100
x 10g
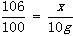 ,x=10.6g
,x=10.6g碳酸钠的质量分数=


练习册系列答案
相关题目
学校探究小组为了测定市面销售的某品牌纯碱(杂质为NaCl)中碳酸钠的质量分数,进行了如下实验:
①在三个烧杯中都加入1lg样品及足量的水配成溶液;
②向三个烧杯加入质量不同的CaCl2粉末;(化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl)
③将充分反应后生成的沉淀过滤、洗涤、干燥得到w g的白色同体.实验数据如下:
回答下列问题:
(1)碳酸钠中钠、碳、氧三种元素的质量比(最简比)为 .
(2)将烧杯IlI的滤液蒸干,得到 g固体,该固体由 和 (只填化学式)组成.
(3)样品中碳酸钠的质量分数是多少?
①在三个烧杯中都加入1lg样品及足量的水配成溶液;
②向三个烧杯加入质量不同的CaCl2粉末;(化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl)
③将充分反应后生成的沉淀过滤、洗涤、干燥得到w g的白色同体.实验数据如下:
| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入CaCl2的质量/g | 5.55 | 12 | 15 |
| W/g | 5 | 10 | 10 |
(1)碳酸钠中钠、碳、氧三种元素的质量比(最简比)为
(2)将烧杯IlI的滤液蒸干,得到
(3)样品中碳酸钠的质量分数是多少?
学校探究小组为了测定市面销售的某品牌纯碱(杂质为NaCl)中碳酸钠的质量分数,进行了如下实验:
①在三个烧杯中都加入1lg样品及足量的水配成溶液;
②向三个烧杯加入质量不同的CaCl2粉末;(化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl)
③将充分反应后生成的沉淀过滤、洗涤、干燥得到w g的白色同体.实验数据如下:
回答下列问题:
(1)碳酸钠中钠、碳、氧三种元素的质量比(最简比)为______.
(2)将烧杯IlI的滤液蒸干,得到______g固体,该固体由______和______(只填化学式)组成.
(3)样品中碳酸钠的质量分数是多少?
①在三个烧杯中都加入1lg样品及足量的水配成溶液;
②向三个烧杯加入质量不同的CaCl2粉末;(化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl)
③将充分反应后生成的沉淀过滤、洗涤、干燥得到w g的白色同体.实验数据如下:
| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入CaCl2的质量/g | 5.55 | 12 | 15 |
| W/g | 5 | 10 | 10 |
(1)碳酸钠中钠、碳、氧三种元素的质量比(最简比)为______.
(2)将烧杯IlI的滤液蒸干,得到______g固体,该固体由______和______(只填化学式)组成.
(3)样品中碳酸钠的质量分数是多少?