题目内容
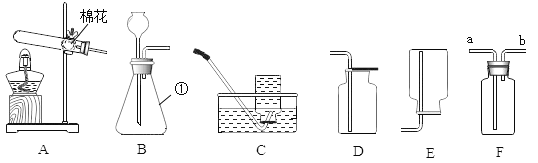
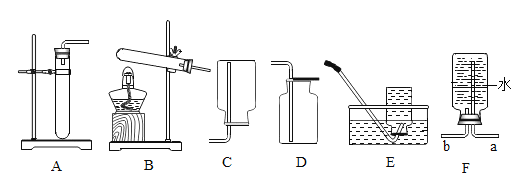
【题目】某化学小组同学用右图所示装置(夹持仪器已略去)做了2个兴趣实验。每次实验时,打开止水夹,均可见C瓶内的水流入D中,B中有气泡逸出。请完成下列空白。

(1)在A处放置燃烧的蜡烛,B中无色溶液变浑浊,写出B中发生反应的化学方程式:___________________________。 蜡烛燃烧生成的气体被吸入B中的原因是________________________。
(2)在A处放置燃烧的蜡烛,若B中盛有紫色石蕊溶液,则变红色,写出B中发生反应的化学方程式:___________________________________。
【答案】 CO2+Ca(OH)2 === CaCO3↓+H2O C瓶内的水流入D中,使C瓶内压强小于大气压,A处气体被吸入B中 CO2+H2O=== H2CO3
【解析】A中的蜡烛燃烧后生成二氧化碳和水,二氧化碳气体与澄清石灰水反应生成碳酸钙沉淀和水,反应方程式为CO2 + Ca(OH)2 == CaCO3 ↓+ H2O;当打开止水夹时,C瓶内的水流入D中,使C瓶内压强小于大气压,A处气体就被吸入B中;
二氧化碳溶于水发生化学反应生成碳酸,碳酸显酸性能使紫色石蕊试液变红,反应方程式为: CO2+H2O=== H2CO3。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】小江同学为了寻找含碳酸钙质量分数超过85%的石灰石,对一样品进行了如下定量实验(石灰石样品中的杂质不与盐酸反应).
实验步骤 | 将适量盐酸加入烧杯中并称重 | 称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | 待反应完全后,称重 |
实验数据 | 烧杯和盐酸的质量为100.0g | 石灰石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
试通过计算,分析该石灰石样品中碳酸钙的质量分数是否符合要求?_____