题目内容
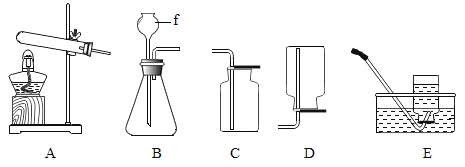
【题目】某化学实验小组想探究氢氧化钙的化学性质,取4支试管分别用A~D编号后,如图进行实验。请回答下列问题:
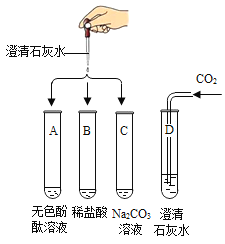
(1)A试管中的现象是___________________________。
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式_________________,该反应的基本类型是________________。
(3)上述实验体现了碱的通性的试管编号是____________(填字母) 。
(4)实验结束后,将4支试管中所有物质倒入一个废波缸,充分反应后,发现烧杯中只得到无色澄清溶液,则烧杯中废液的溶质(指示剂除外)一定有______________(写出化学式),为了确定可能有的物质是否存在,还需要补充的实验是________________________。
【答案】溶液变红 ![]() 复分解反应 ABD NaCl、CaCl2 取少量废液于试管中,加入锌粉,观察是否有气泡产生,有气泡,说明含有盐酸,无气泡产生,说明不含盐酸
复分解反应 ABD NaCl、CaCl2 取少量废液于试管中,加入锌粉,观察是否有气泡产生,有气泡,说明含有盐酸,无气泡产生,说明不含盐酸
【解析】
(1)氢氧化钙显碱性,能使无色酚酞试液变红,故A试管中的现象是:溶液变红;
(2)A试管,氢氧化钙显碱性,能使无色酚酞试液变红;B试管,氢氧化钙与稀盐酸反应生成氯化钙和水,无明显现象,该反应的化学方程式为:![]() ;该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应;C试管碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,有白色沉淀产生;D试管澄清石灰水变浑浊;故填:
;该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应;C试管碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,有白色沉淀产生;D试管澄清石灰水变浑浊;故填:![]() 、复分解反应;
、复分解反应;
(3)A、氢氧化钙显碱性,碱能使无色酚酞试液变红,体现了碱的通性,符合题意;
B、氢氧化钙能与稀盐酸反应生成了氯化钙和水,体现了碱的通性,符合题意;
C、氢氧化钙与碳酸钠反应生成碳酸钙和氢氧化钠,不能体现碱的通性,不符合题意;
D、氢氧化钙能与二氧化碳反应生成碳酸钙和水,体现了碱的通性,符合题意。
故选ABD;
(4)A试管无色酚酞变红,B试管氢氧化钙与稀盐酸反应生成氯化钙和水,C试管碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,D试管氢氧化钙与二氧化碳反应生成碳酸钙和水,实验结束后,将4支试管中所有物质倒入一个废波缸,充分反应后,发现烧杯中只得到无色澄清溶液,无色,说明不含碱性物质,反应生成的氢氧化钠与盐酸反应生成了氯化钠和水,澄清溶液,说明碳酸钙和盐酸反应生成了氯化钙、二氧化碳和水,故烧杯中废液的溶质(指示剂除外)一定有:NaCl、CaCl2;
稀盐酸可能过量,故废液中可能含有稀盐酸,为了确定稀盐酸是否存在,可取少量废液于试管中,加入锌粉,观察是否有气泡产生,有气泡,说明含有盐酸,无气泡产生,说明不含盐酸。