题目内容
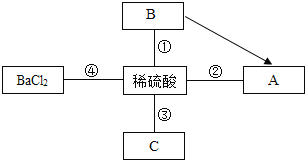
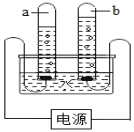
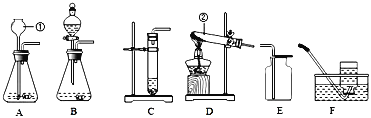
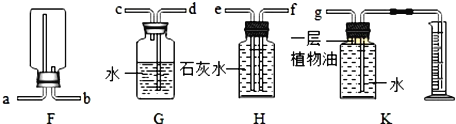
【题目】某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了如图两个实验:
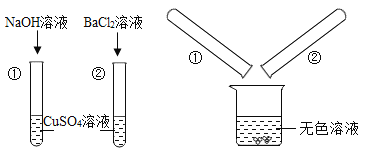
实验一:
实验二:
组合序号 | ① | ② | ③ |
组合的溶液 |
|
|
|
(实验一):把试管①②中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液。
(1)根据上述现象判断,试管①中一定反应完全的是__________(填化学式);写出试管②中发生反应的化学方程式____________________;混合后得到蓝色沉淀一定发生反应的化学方程式____________________。
(2)混合后所得无色溶液中一定含有的溶质是______________(填化学式,下同)可能含有的溶质是____________________。
(实验二):
(3)在组合①、②、③中,组合_________无明显现象,但它们的实质不同,为了证明实质不同,小夕在实验过程中使用了酚酞试液。
(4)实验结束后把3个组合反应后的溶液混合,混合后溶液也显无色。混合后所得溶液中除酚酞外溶质的组成可能是___________(填化学式)。
(结论):
(5)复分解反应发生的条件是:生成物中有____________________生成。
【答案】![]()
![]()
![]() NaCl、
NaCl、![]() NaOH ①② NaCl和
NaOH ①② NaCl和![]() 或
或![]() 、NaCl和
、NaCl和![]() 水或气体或沉淀
水或气体或沉淀
【解析】
探究“复分解反应发生的条件”:
实验一:试管①中氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,试管②中氯化钡与硫酸铜反应生成硫酸钡沉淀和氯化铜,把试管①②中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液,说明原试管①中氢氧化钠过量,试管②中氯化钡完全反应,试管①②上层清液混合发生的反应为氢氧化钠和氯化铜反应生成氢氧化铜蓝色沉淀和氯化钠,氯化铜完全反应,氢氧化钠可能有剩余。
(1)根据上述现象判断,试管①中剩余有氢氧化钠,则试管①中一定反应完全的是![]() ;试管②中发生反应的化学方程式为
;试管②中发生反应的化学方程式为![]() ;混合后得到蓝色沉淀一定发生氢氧化钠和氯化铜反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式为
;混合后得到蓝色沉淀一定发生氢氧化钠和氯化铜反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式为![]() 。
。
(2)混合后所得无色溶液中一定含有的溶质是NaCl和![]() ,可能含有的溶质是NaOH。
,可能含有的溶质是NaOH。
实验二:
组合①:![]() 溶液和
溶液和![]() 溶液,二者反应生成水和硫酸钠,无明显现象;
溶液,二者反应生成水和硫酸钠,无明显现象;
组合②:![]() 溶液和
溶液和![]() 溶液,二者不反应,无明显现象
溶液,二者不反应,无明显现象
组合③:![]() 溶液和
溶液和![]() 溶液,二者反应生成硫酸钠、二氧化碳和水,有气泡产生;
溶液,二者反应生成硫酸钠、二氧化碳和水,有气泡产生;
(3)在组合①、②、③中,组合①②无明显现象,但它们的实质不同,为了证明实质不同,小夕在实验过程中使用了酚酞试液。
(4)实验结束后把3个组合反应后的溶液混合,混合后溶液也显无色。氢氧化钠和碳酸钠溶液都能使酚酞变红,则说明混合后所得溶液显中性或酸性,故混合后所得溶液中除酚酞外溶质的组成可能是:①NaCl和![]() ;②
;②![]() 、NaCl和
、NaCl和![]() 。
。
结论:
(5)复分解反应发生的条件是:生成物中有水或气体或沉淀生成。

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案