题目内容
【题目】写出下列化学方程式:
①木炭还原氧化铜______;
②检验二氧化碳______;
③碳还原氧化铁______;
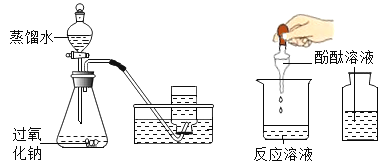
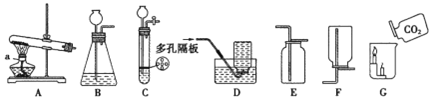
④实验室制取二氧化碳______;
⑤二氧化碳与碳反应______。
【答案】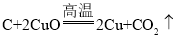
![]()
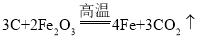
![]()
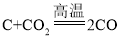
【解析】
①木炭在高温的条件下还原氧化铜,生成铜和二氧化碳,反应的化学方程式为: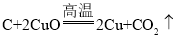 ;
;
②检验二氧化碳气体用澄清的石灰水,二氧化碳与氢氧化钙反应,生成碳酸钙沉淀和水,反应的化学方程式为:![]() ;
;
③碳在高温的条件下还原氧化铁,生成铁和二氧化碳,反应的化学方程式为: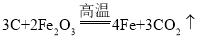 ;
;
④实验室常用块状药品大理石或石灰石与液体药品稀盐酸反应,生成氯化钙、水、二氧化碳,反应的化学方程式是:![]() ;
;
⑤二氧化碳与碳在高温的条件下反应,生成一氧化碳,反应的化学方程式为: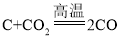 。
。

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案【题目】盐酸硫酸和硝酸是三种常用的酸,为什么初中化学只介绍了盐酸和硫酸,没有介绍硝酸呢?兴趣小组同学在实验室发现一瓶硝酸,发现硝酸保存在棕色试剂瓶中,小组的同学对此产生了好奇,并对硝酸的部分性质进行如下探究。
[查阅资料]①棕色试剂瓶常用于保存见光易分解的物质;②NO是无色气体,能与空气中的氧气迅速反应生成NO2,NO2是红棕色气体,低温时转化成液体N2O4;③相同条件下,气体的体积比等于气体分子数目之比;④无水氯化钙可干燥NO、NO2、H2、O2等。
[提出问题]硝酸具有哪些化学性质?
[提出猜想]猜想一:硝酸不稳定,易分解;
猜想二:稀硝酸可与铁反应产生氢气;
猜想三:硝酸能与氢氧化钠反应。
[实验探究]
实验操作 | 实验现象 | 实验结论 | |
① | 取少量浓硝酸于试管中,用酒精灯加热 | 产生红棕色气体 | 猜想一正确 |
② | 向稀硝酸中加入少量铁粉 | 有气泡产生,气体在试管口由无色变为红棕色,铁粉逐渐溶解,得到黄色溶液 | 猜想二不正确 |
③ | 向稀硝酸中滴加氢氧化钠溶液 | 无明显现象 | 猜想三不正确 |
[交流讨论](1)小明认为铁与稀硝酸反应产生的气体是NO,他的依据是___________________。
(2)小江认为实验③的结论不严谨,他重新设计方案验证猜想三,请补充小江的实验报告:
实验操作 | 实验现象 | 实验结论 |
_______________。 | _______________。 | 猜想三正确 |
[继续探究]为验证硝酸分解的气体产物,在老师的指导下,小组同学设计如图装置:
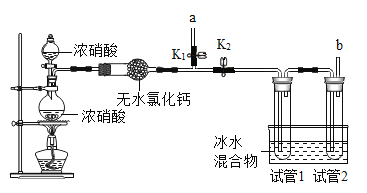
[实验步骤] I.关闭K2,打开K,加热观察到有红棕色气体产生,当有红棕色气体由导管口a逸出时,将带火星的木条放在导管口a处,观察到木条复燃;
II.打开K2,关闭K1,一段时间后,试管1中出现无色液体,试管2中无明显现象,将带火星的木条放在导管口b处,观察到木条复燃。经进一步实验确认浓硝酸分解的产物有三种,则浓硝酸分解产生的气体为____________。
[知识拓展]小江分析上述实验后,认为二氧化氮具有助燃性,请说明理由_____________。
【题目】铁在自然界中以铁矿石形式分布很广。铁不仅年产量最高,且应用最为广泛。请回等下列问题:
(1)亮亮化学兴趣小组用下图所示装置进行一氧化碳还原氧化铁的模拟炼铁实验。
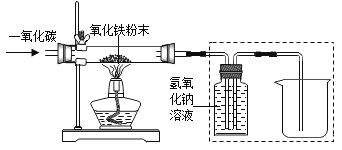
当玻璃管内固体粉来由红棕色全部变为黑色时停止加热。亮亮认为该黑色固体全部是铁:但同学小华提出了质疑,她将该黑色固体研磨后用磁铁吸引,发现全部被吸引。
(提供费料)a.Fe2O3是在一定温度下逐步失去其中的氧,依次生成Fe3O4、FeO和Fe
b.如表
镁及铁的氧化物 | 铁粉 | 氧化亚铁 | 氧化铁 | 四氧化三铁 |
颜色 | 黑 | 黑 | 红棕 | 黑 |
能否被磁铁吸引 | 能 | 否 | 否 | 能 |
c.酒精灯火焰的温度一般为400℃-700℃左右
(提出问题)该反应中生成的黑色物质是什么?
(大胆猜想)你认为黑色物质的组成可能是:
①_____;
②_____;
③_____;
(实验方案)④上图虚线右侧部分装置的作用是_____。
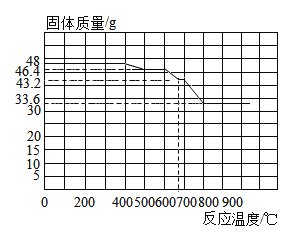
⑤在一定温度下,记录实验所得数据如下表所示,通过计算确定黑色固体物质的化学式为_____。
玻璃管质量 | 玻璃管-内盛固体 | |
反应前质量 | 反应后质量 | |
50.0g | 56.0g | 55.8g |
(2)洋洋同学也找到一些铁锈样品进行实验视究,他所用的实验装置如图所示
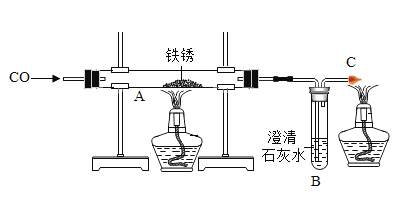
⑥C处的化学反应方程式_____,待反应完成后,将所得黑色固体物质放入足量的稀硫酸中。小明认为该物质中并不含铁,他的依据是:_____。
⑦为了解释这一反常现象,他查到某炼铁厂对氧化铁和一氧化碳进行的热反应分析,根据相关的数据绘制图像如下。通过分析确定实验没有得到铁的主要原因是_____,你的改进方法是_____。