题目内容
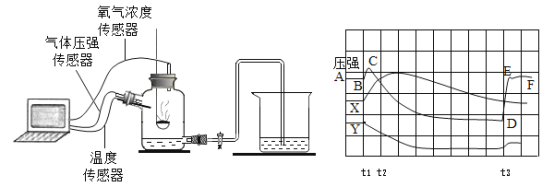
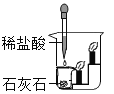
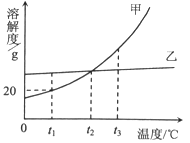
【题目】某化学小组的同学们对一份固体样品进行了探究.通过实验已确定该样品由氧 化铁和铁粉混合而成.他们取了 7.2g 固体样品,用图 1 所示的装置继续实验,测定的部分数据如图 2 所示。
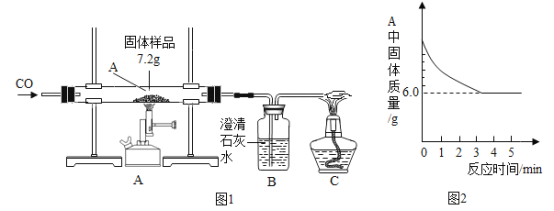
请计算:
(1)写出硬质玻璃管内的实验现象_____;
(2)该样品中含有氧化铁的质量为_____g;
(3)若澄清石灰水足量,反应结束后,装置 B 增重质量为多少?_____(写出具体计算步骤)
【答案】混合固体红色部分变黑色 4 3.3g
【解析】
样品的质量为7.2g,通入一氧化碳气体,一氧化碳与氧化铁反应,结合图2,反应后固体质量为6g,减少了1.2g,减少的质量为氧化铁中氧元素的质量。
(1)硬质玻璃管内发生的反应是一氧化碳和氧化铁在高温条件下生成铁和二氧化碳,实验现象混合固体红色部分变黑色。
(2)该样品中含有氧化铁的质量为:![]() 。
。
(3)解:设生成二氧化碳的质量为X。

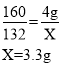
答:装置 B 增重质量3.3g。

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
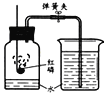
【题目】如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )
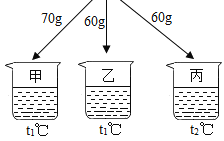
温度(℃) | t1 | t2 |
KNO3的溶解度(g/100g水) | 60 | 90 |
A.甲、乙、丙均为饱和溶液B.乙升温至t2℃,溶液质量增加
C.甲、乙、丙溶液中溶质质量相等D.丙溶液的溶质质量分数是60%
【题目】实验是学习化学的重要方法,下列实验设计不能实现相应实验目的的是
选项 | 实验目的 | 实验设计 | 选项 | 实验目的 | 实验设计 |
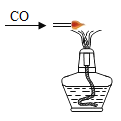
A | 除去CO2中少量的CO |
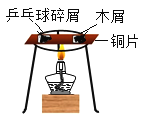
| B | 探究不同物质的着火点不同 |
|
C | 探究CO2的化学性质 |
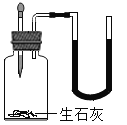
| D | 探究生石灰与水反应是否放热 |
|
A.AB.BC.CD.D