题目内容
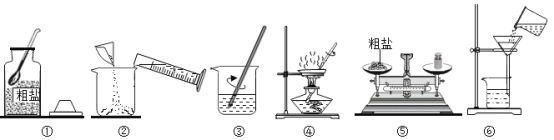
【题目】按要求填写表中空格:
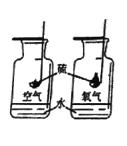
实验目的:探究影响硫燃烧剧烈程度的因素
如图,分别将相同质量的硫粉在空气和氧气中燃烧。
(1)硫在空气里燃烧的符号表达式为__________________。
(2)集气瓶中事先加少量水的目的是_________________________
(3)硫在氧气中燃烧的现象是发出明亮的__________色火焰,放热,产生____________。
(4)通过对比两瓶中燃烧的现象,可以说明影响硫燃烧剧烈程度的因素是________。
【答案】S+O2![]() SO2 吸收二氧化硫,防止污染环境 明亮的蓝紫色 产生一种刺激性气味的气体 氧气的浓度
SO2 吸收二氧化硫,防止污染环境 明亮的蓝紫色 产生一种刺激性气味的气体 氧气的浓度
【解析】
(1)硫在空气里燃烧生成了二氧化硫,符号表达式为:S+O2![]() SO2。
SO2。
(2)由于硫在空气里燃烧生成了二氧化硫有毒,能污染空气,所以集气瓶中事先加少量水的目的是:吸收二氧化硫,防止污染环境;
(3)硫在氧气中燃烧的现象是:发出明亮的蓝紫色火焰,放热,产生一种刺激性气味的气体。
(4)通过对比两瓶中燃烧的现象,可以说明影响硫燃烧剧烈程度的因素是氧气的浓度。

【题目】二氧化锰可作过氧化氢溶液分解的催化剂,兴趣小组想探究过氧化氢分解有没有其他催化剂,以及影响过氧化氢分解速率的因素除催化剂外还有哪些。
Ⅰ.(提出问题)氧化铁能否作过氧化氢分解的催化剂?如果能,其催化效果如何?
(实验探究)
实验步骤 | 实验现象 |
①分别取5mL5%过氧化氢溶液放入A、B两支试管中,向A中加入1g氧化铁粉末,并分别在A、B试管中插入带火星的木条,观察现象。 | A试管中产生气泡,带火星的木条复燃,B试管中无明显现象。 |
②待A中没有现象发生时,重新加入过氧化氢溶液,把带火星的木条伸入试管,如此反复3次。 | 试管中均产生气泡,带火星的木条均复燃。 |
③将步骤②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量为ag。 |
|
④分别取5mL5%过氧化氢溶液放入C、D两支试管中,向C中加入1g氧化铁粉末,向D中加入1g二氧化锰粉末,观察现象。 |
|
(实验结论)
(1)步骤②证明氧化铁的___在反应前后没有发生变化;③中如果a=___,证明氧化铁的___在反应前后没有发生变化。由①②③可知,氧化铁可以作过氧化氢分解的催化剂。
(2)写出试管A中发生反应的文字表达式___。
(实验评价)
设计实验步骤④的目的是___,若观察到D试管中产生气泡的速率比C试管中快,由此可以得到的结论是___。
Ⅱ.探究过氧化氢溶液浓度对过氧化氢分解速率的影响。
(交流讨论)可以通过测定相同条件下不同浓度过氧化氢溶液___来探究。
A 产生相同体积氧气的时间 B 产生氧气的总体积 C 单位时间内产生氧气的体积
(实验探究)
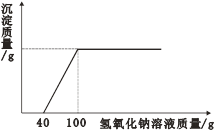
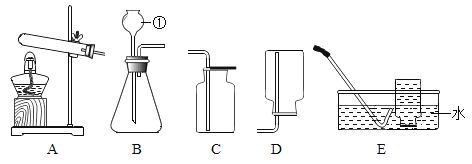
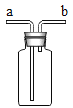
按图1装置进行实验:水浴温度控制在21℃,二氧化锰均为0.5g,过氧化氢溶液均为5mL,三颈瓶容积为250mL,恒压漏斗(漏斗的支管与三颈瓶相连)的作用是使过氧化氢溶液自行下滴。数字传感器数据绘制图像如图2、图3。
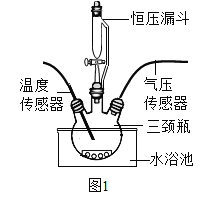

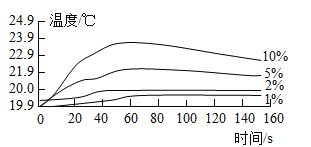
(实验结论)
图2说明过氧化氢溶液浓度与反应速率之间的关系是____,结合图3,以10%H2O2溶液为例分析,三颈瓶内气压后来慢慢降低的原因是_____。