题目内容
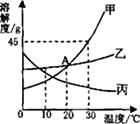
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)A点的含义是______________。
(2)在30℃时,向30g甲物质中加入50g水,充分溶解后所得溶液是____________溶液(填“饱和”或“不饱和”)。
(3)若乙中混有少量甲,最好采用_________的方法提纯乙。
(4)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的物质是____。
【答案】20℃时,甲和乙溶解度相等 饱和 蒸发结晶 丙
【解析】
(1)由溶解度曲线可知,A点是甲乙曲线的交点,含义是:20℃时,甲和乙溶解度相等;
(2)由溶解度曲线可知,在30℃时,甲物质的溶解度是45g,向30g甲物质中加入50g水,充分溶解后只能溶解22.25g,所得溶液是饱和溶液;
(3)由于乙的溶解度随温度的变化不大,甲的溶解度水温度的升高而增大,若乙中混有少量甲,最好采用蒸发结晶的方法提纯乙;
(4)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,由于甲乙的溶解度随温度的降低二减小,要析出晶体,溶质的质质量分数要减小,丙的溶解度随温度的降低二增大,则其溶质质量分数不变。

【题目】某化学兴趣小组同学,用盐酸和氢氧化钠进行“酸碱中和反应”的探究,进行一段时间后发现没有明显变化,询问老师才知道忘记滴加指示剂。因此,他们停止实验,并在老师的指导下对烧杯内的溶液中的溶质的成分进行探究。
(提出问题)该烧杯内的溶质是什么?
(猜想假设)猜想一:NaCl 猜想二:NaCl和HCl
猜想三:NaCl和NaOH 猜想四:NaCl、NaOH和HCl
同学们讨论后一致认为猜想四不合理,请你说出不合理的理由______________________(用化学方程式表示)。
(查阅资料)NaCl溶液呈中性。
(实验探究)兴趣小组甲、乙、丙三位同学分别设计了如下的实验方案,请你帮助他们完成实验报告的相关内容。
实验方案 | 实验现象 | 实验结论 |
甲同学取少量烧杯内的溶液于试管中,滴入酚酞试液 | 溶液无变化 | 猜想一成立 |
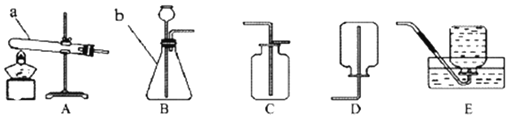
乙同学另取少量烧杯内的溶液于试管中,加入_______。 | 有气泡生成 | 猜想二成立 |
丙同学另取少量烧杯内的溶液于试管中,滴加适量的CuSO4溶液 | 没有蓝色沉淀产生 | 猜想____不成立 |
(评价反思)老师看了甲、乙、丙三位同学的实验报告,指出甲同学的实验结论不准确,请你分析甲同学实验结论不准确的原因:___________。
(得出结论)猜想二成立
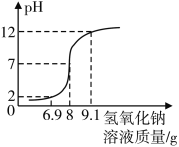
(拓展延伸)某同学在进行酸碱中和滴定实验时,测得溶液的pH变化如下图1所示,请回答下列问题:

(1)由图1可知,该同学实验操作是________________。
A.将盐酸滴入氢氧化钠溶液中
B.将氢氧化钠溶液滴入盐酸中
(2)由图1可知,在b点处溶液中溶质是______________________。
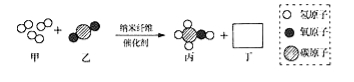
(3)图2为盐酸和氢氧化钠溶液反应的微观过程,从微粒的角度分析,此反应的微观实质_______________(合理答案即可)。