题目内容
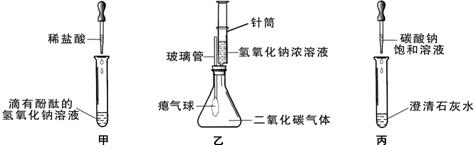
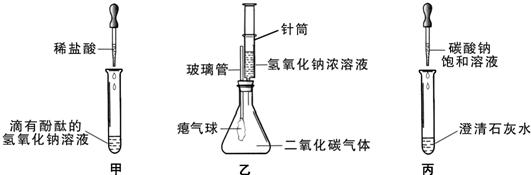
同学们在学习碱的化学性质时,进行了如图所示的实验.
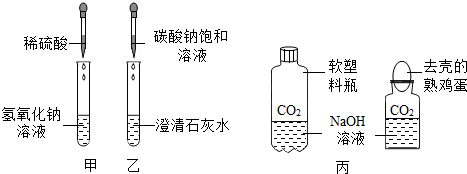
(1)写出甲实验中反应的化学方程式
(2)乙实验中可观察到的现象是
(3)某兴趣小组同学将制得的CO2分别通入澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.为探究CO2和NaOH是否发生了化学反应?
①小明设计了丙图所示的两个实验来验证CO2与NaOH发生了化学反应.实验现象为:前一个软塑料瓶变瘪,后一个“瓶吞鸡蛋”.
小虎同学认为上述实验是可行的,其共同原理是
小雯同学提出质疑,她认为上述实验还不足以说明CO2和NaOH发生了反应,其理由是
小明同学针对小雯的质疑又补充了一个对照实验,这个实验是
②小虎向甲实验后变瘪塑料瓶的溶液中加入

(1)写出甲实验中反应的化学方程式
2NaOH+H2SO4═Na2SO4+2H2O
2NaOH+H2SO4═Na2SO4+2H2O
.(2)乙实验中可观察到的现象是
产生白色沉淀
产生白色沉淀
.(3)某兴趣小组同学将制得的CO2分别通入澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.为探究CO2和NaOH是否发生了化学反应?
①小明设计了丙图所示的两个实验来验证CO2与NaOH发生了化学反应.实验现象为:前一个软塑料瓶变瘪,后一个“瓶吞鸡蛋”.
小虎同学认为上述实验是可行的,其共同原理是
氢氧化钠溶液能与CO2发生反应,瓶内气压降低
氢氧化钠溶液能与CO2发生反应,瓶内气压降低
小雯同学提出质疑,她认为上述实验还不足以说明CO2和NaOH发生了反应,其理由是
CO2能溶于水,也能使瓶内气压降低
CO2能溶于水,也能使瓶内气压降低
.小明同学针对小雯的质疑又补充了一个对照实验,这个实验是
将氢氧化钠溶液换成等体积的水,做同样的实验,看现象是否有差别
将氢氧化钠溶液换成等体积的水,做同样的实验,看现象是否有差别
②小虎向甲实验后变瘪塑料瓶的溶液中加入
稀盐酸
稀盐酸
,观察到有气泡产生
有气泡产生
现象,从而证明CO2与NaOH已经发生了反应.分析:(1)根据反应物、生成物和质量守恒定律写出方程式;
(2)根据碳酸钠和氢氧化钙反应生成不溶于水的碳酸钙来描述反应现象;
(3)①根据氢氧化钠溶液能与CO2发生反应,瓶内气压降低分析;根据二氧化碳能溶于水分析疑点;根据疑点可以做一个对比试验解析疑点;
②加入一种试剂与CO2与NaOH反应生成的产物反应产生明显的现象,即可证明CO2与NaOH反应了.
(2)根据碳酸钠和氢氧化钙反应生成不溶于水的碳酸钙来描述反应现象;
(3)①根据氢氧化钠溶液能与CO2发生反应,瓶内气压降低分析;根据二氧化碳能溶于水分析疑点;根据疑点可以做一个对比试验解析疑点;
②加入一种试剂与CO2与NaOH反应生成的产物反应产生明显的现象,即可证明CO2与NaOH反应了.
解答:解:(1)氢氧化钠和稀硫酸反应生成硫酸钠和水,反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O
(2)碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,因为碳酸钙不溶于水,所以溶液变浑浊,故填:产生白色沉淀
(3)①因为氢氧化钠溶液能与CO2发生反应,瓶内气压降低,大气压就把软塑料瓶压瘪,把鸡蛋压进瓶内;因为CO2能溶于水,也能使瓶内气压降低,会产生同样的效果,所以这是产生二氧化碳和氢氧化钠是否反应的一个疑点;为了这个疑点,可以做一个对比试验,就是将氢氧化钠溶液换成等体积的水,做同样的实验,看现象是否有差别.故填:氢氧化钠溶液能与CO2发生反应,瓶内气压降低;CO2能溶于水,也能使瓶内气压降低;将氢氧化钠溶液换成等体积的水,做同样的实验,看现象是否有差别
②因为二氧化碳和氢氧化钠反应生成碳酸钠,只要验证有碳酸钠存在就可证明二氧化碳和氢氧化钠反应了,可以加入稀盐酸,有气泡生成即可说明.故填:稀盐酸;有气泡产生
(2)碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,因为碳酸钙不溶于水,所以溶液变浑浊,故填:产生白色沉淀
(3)①因为氢氧化钠溶液能与CO2发生反应,瓶内气压降低,大气压就把软塑料瓶压瘪,把鸡蛋压进瓶内;因为CO2能溶于水,也能使瓶内气压降低,会产生同样的效果,所以这是产生二氧化碳和氢氧化钠是否反应的一个疑点;为了这个疑点,可以做一个对比试验,就是将氢氧化钠溶液换成等体积的水,做同样的实验,看现象是否有差别.故填:氢氧化钠溶液能与CO2发生反应,瓶内气压降低;CO2能溶于水,也能使瓶内气压降低;将氢氧化钠溶液换成等体积的水,做同样的实验,看现象是否有差别
②因为二氧化碳和氢氧化钠反应生成碳酸钠,只要验证有碳酸钠存在就可证明二氧化碳和氢氧化钠反应了,可以加入稀盐酸,有气泡生成即可说明.故填:稀盐酸;有气泡产生
点评:本题主要考查了学生对于碱的化学性质的掌握情况,碱的化学性质很重要,是一个经常出现的考点,应熟练掌握.

练习册系列答案
相关题目