��Ŀ����
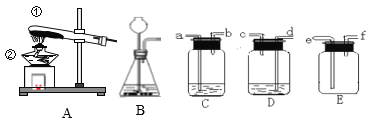
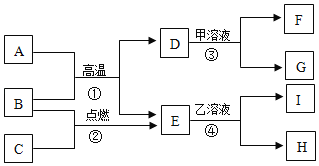
����Ŀ���������ͼ��ʾ��ʵ��װ��ͼ��գ�

(1)ͼ�������ڵ�����Ϊ__��
(2)ʵ������Bװ����ȡ����ʱ�������ٵ�������___(дһ�㼴��)��
(3)���д���ʯ��̼���Ʒ�ĩ��ϡ���ᡢϡ���ᣬ��ѡ����ʵ����ʣ���Cװ����ȡCO2���壬�䷴Ӧ�Ļ�ѧ����ʽΪ____���ڷ�Ӧ�����У�ʹ��Ӧֹͣ�IJ�����____��
(4)����(NH3)��һ�ּ�������ˮ�����壬ʵ���ҳ��ü����Ȼ�狀��������ƹ�������ķ�������ȡ����Ӧ����Ϊ������ˮ�Լ�һ���Σ��䷴Ӧ�Ļ�ѧ����ʽΪ___����ȡ���ռ�������װ�������____������Gװ���ռ�����������Ӧ��__�˵���(ѡ����a������b��)��
���𰸡�����ƿ ����Һ���������ʣ��Ӷ�����������������( ������������Ĵ𰸶�����) CaCO3+2HCl=CaCl2+H2O+CO2![]() �رջ��� 2NH4Cl + Ca(OH)2
�رջ��� 2NH4Cl + Ca(OH)2![]() CaCl2+ 2NH3�� + 2H2O AF��AG b
CaCl2+ 2NH3�� + 2H2O AF��AG b
��������
��1��ͼ�н����ڵ�����Ϊ����ƿ��
��2��ʵ������Bװ����ȡ����ʱ������Bװ�ò��õ��Ƿ�Һ©������������������ӹ���������Һ������Һ��ĵμ��ٶȣ�����֮�������ɣ�
��3��ʵ��������ʯ��ʯ�����ʯ��ϡ������ȡ������̼��ʯ��ʯ����Ҫ�ɷ���̼��ƣ�̼��ƺ�ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼������ʽΪ��CaCO3+2HCl=CaCl2+H2O+CO2������Cװ����ȡCO2���壬Ҫʹ��Ӧֹͣ�ģ��ر��ұߵĵ��ܣ���������ʹװ����ѹǿ���Ӷ��ų�Һ��ʹ��Һ����ֹͣʵ�顣
��4��ʵ���ҳ��ü����Ȼ�狀��������ƹ�������ķ�������ȡ����Ӧ�ķ���ʽΪ��2NH4Cl + Ca(OH)2![]() CaCl2+ 2NH3�� + 2H2O����Ӧ�ﶼ�ǹ��壬��Ӧ�����Ǽ��ȣ���˲��÷���װ����A���������ܶ�С�ڿ����ܶȣ�������ˮ����˲��ܲ�����ˮ���ռ�����Gװ���ռ�����ʱ�������b�˽���
CaCl2+ 2NH3�� + 2H2O����Ӧ�ﶼ�ǹ��壬��Ӧ�����Ǽ��ȣ���˲��÷���װ����A���������ܶ�С�ڿ����ܶȣ�������ˮ����˲��ܲ�����ˮ���ռ�����Gװ���ռ�����ʱ�������b�˽���

 ������������Ծ�ϵ�д�
������������Ծ�ϵ�д� �������Ӳ�ϵ�д�
�������Ӳ�ϵ�д�����Ŀ����������ͭ�dz��������ֽ����������е�����Ʒ��ͭ������һ�㲻�÷��⣬������Ʒ����������
��������⣩�����ֽ����Ļ��ǿ����������أ�
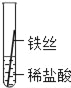
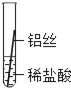
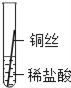
��ʵ��̽����ͬѧ�ǽ���ϸ��ͬ����˿����˿��ͭ˿�ֱ������������Ũ�ȵ�ϡ������Һ�У�
���� |
|
|
|
Ƭ�̺����� | ���������������� | ������ | ������ |
�����Ӻ����� | ���������������� | ���ٲ����������� | ������ |
�����۽�����
�����������ó����ֽ����Ļ����ǿ������˳����_____��
��˿����ϡ�����ʵ���У������������ʱ��仯�����ֵ������²�ù����л�������ʲô��Ӧ��_____����������������
����˼�Ľ�����������ϡ���ᷴӦ
����֤����������ʵ��ǰ����Խ������������Ĵ�����_____��
��ͬѧ�����ֻ��һ֧ʢ������ϡ������Թܣ�ֻ���������˿�IJ���˳��Ҳ��֤�����ֽ����Ļ��˳�����������˿�IJ���˳�����Ϊ_____����һ��˳�ɣ���
����չǨ�ƣ���һ�����������۷��뺬����������������ͭ�Ļ����Һ�У���ַ�Ӧ���ˡ����˳��Ĺ����еμ�ϡ���ᣬ���������ݲ�����
��Һ��һ�����е�������_____���ѧʽ����
�ù����в�������ʱ��һ�������ķ�Ӧ�ķ���ʽΪ_____��