题目内容
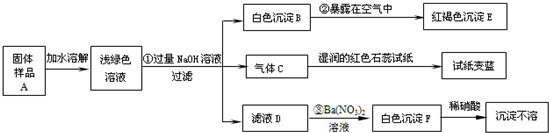
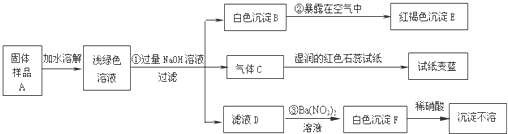
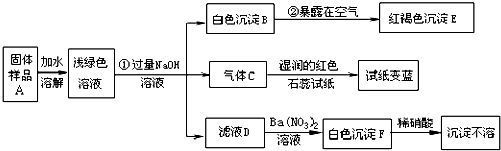
某地新建一化工厂有一种产品属于“复盐”,该产品可用作铁树、棕榈等花木的肥料.某化学兴趣小组探究该产品的组成,进行了如下实验:[查阅资料获知:“复盐”是指由两种阳离子和一种酸根离子组成的盐.如光卤石(KCl?MgCl2?6H2O)].已知白色Fe(OH)2在潮湿的空气中可转化成Fe(OH)3试回答下列问题: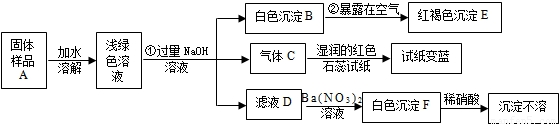
(1)写出下列物质的化学式:C;F.
(2)上述探究结果说明样品A中含有的离子有、、.
(3)写出B→E的化学方程式.
【答案】分析:在做推断题时,首先找出解决这一题的题眼,然后由题眼推断出其它物质.如这一题的题眼是气体C使湿润的红色石蕊试纸变蓝色,所以C为氨气.
解答:解:滤液D滴加硝酸钡,得白色沉淀F,F也不溶于硝酸,所以F为硫酸钡.也就是说在滤液D中含有硫酸根离子.气体C使湿润的红色石蕊试纸变蓝色,所以C为氨气.所以在浅绿色溶液中含有铵根离子.又因溶液显绿色,所以也含有亚铁离子.又因白色Fe(OH)2在潮湿的空气中可转化成Fe(OH)3,所以白色沉淀B为氢氧化亚铁,红褐色深沉E为氢氧化铁.
由以上我们可以得出在固体A中一定含有亚铁离子、铵根离子、硫酸根离子.
故答案为:
(1)NH3;BaSO4
(2)NH4+、Fe2+、SO42-
(3)4Fe(OH)2+O2+2H2O═4Fe(OH)3
点评:在初中我们所接触到的即不溶于水也不溶于酸的沉淀有两种.一种是氯化银、一种是硫酸钡.在初中我们所接触到的显碱性的气体只有氨气.
解答:解:滤液D滴加硝酸钡,得白色沉淀F,F也不溶于硝酸,所以F为硫酸钡.也就是说在滤液D中含有硫酸根离子.气体C使湿润的红色石蕊试纸变蓝色,所以C为氨气.所以在浅绿色溶液中含有铵根离子.又因溶液显绿色,所以也含有亚铁离子.又因白色Fe(OH)2在潮湿的空气中可转化成Fe(OH)3,所以白色沉淀B为氢氧化亚铁,红褐色深沉E为氢氧化铁.
由以上我们可以得出在固体A中一定含有亚铁离子、铵根离子、硫酸根离子.
故答案为:
(1)NH3;BaSO4
(2)NH4+、Fe2+、SO42-
(3)4Fe(OH)2+O2+2H2O═4Fe(OH)3
点评:在初中我们所接触到的即不溶于水也不溶于酸的沉淀有两种.一种是氯化银、一种是硫酸钡.在初中我们所接触到的显碱性的气体只有氨气.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目