题目内容
【题目】如图是化学兴趣小组的同学设计和改进的实验装置,请你参与他们的探究活动.回答下列问题:
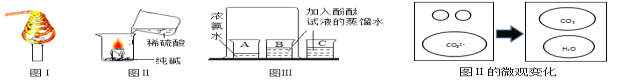
(1)图Ⅰ:我参与我快乐,在探究灭火的原理时我用一根粗铜丝绕成线圈罩在蜡烛的火焰上,火焰很快熄灭.我用了金属线圈灭火的原理是__________;
(2)图Ⅱ在铺有一层纯碱粉末的烧杯中点燃一支蜡烛后加入适量蒸馏水充分溶解,然后沿着烧杯壁缓缓倒入稀硫酸至恰好完全反应。
①观察到的现象是________,写出反应的化学方程式____________;
②此反应中发生相互作用的微粒是___________(微粒符号),发生相互作用的微粒个数比是_________。
(3)图Ⅲ:小组同学在烧杯A中加入10mL浓氨水;在烧杯B、C中都加入20mL蒸馏水,并分别滴加几滴酚酞试液于蒸馏水中,得到无色溶液.用一只大烧杯把A、B两烧杯罩在一起,几分钟后,溶液颜色变成红色的烧杯是 ____(选填“A”、“B”或“C”),请你用分子的知识解释烧杯中溶液变红的原因____ 。
【答案】降低环境温度到可燃物的着火点以下气泡产生,然后燃着的蜡熄灭H2SO4+Na2CO3==Na2SO4+CO2↑+H2OH+ ,CO32-2:1或1:2B 微粒在不断远动
【解析】
(1)铜的导热性良好,很容易吸收周围热量,将环境温度降到可燃物的着火点以下,导致火焰熄灭;
(2)①稀硫酸与纯碱生成二氧化碳气体,故有气泡产生,又因二氧化碳不支持燃烧能观察到燃着的蜡熄灭;化学反应方程式为H2SO4+Na2CO3==Na2SO4+CO2↑+H2O;②根据化学方程式和图二微观变化可知其反应实质是氢离子和碳酸根离子反应生成二氧化碳和水,离子符号为H+ ,CO32-;通过观察可发现氢离子和碳酸根离子个数比为2:1,故填2:1或1:2;
(3)因为浓氨水具有很强挥发性,滴有酚酞的蒸馏水会因浓氨水不断扩散发生接触导致颜色变红,故填B;扩散现象的本质是微观粒子不断运动。

 步步高达标卷系列答案
步步高达标卷系列答案