题目内容
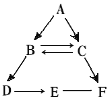
【题目】某化学实验室从含少量硝酸锌的硝酸铝废液中提取贵金属Ag,其主要操作流程如图:
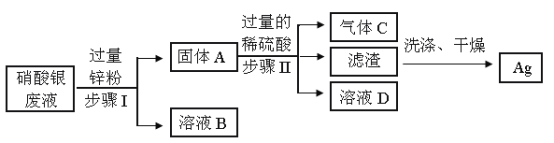
(1)步骤Ⅰ的实验操作中,玻璃棒的作用是_____。
(2)步骤Ⅱ中发生的化学反应方程式_____。
(3)由上述实验可得出锌、银、氢由强到弱的活动顺序为_____。
(4)若往溶液D中加入足量某物质,可得到只含一种溶质的溶液,则该物质可能是_____。
A Zn B ZnO C Zn(OH)2 D ZnCO3
【答案】引流 Zn+H2SO4=H2↑+ZnSO4 ZnHAg ABCD
【解析】
过量锌粉能与硝酸银溶液反应生成硝酸锌溶液和银,固体A为银和锌的混合物,溶液B为硝酸锌溶液,锌能与过量的稀硫酸反应生成硫酸锌溶液和氢气,铜不与稀硫酸反应,则气体C为氢气,溶液D为硫酸锌和硫酸的混合溶液。
(1)步骤Ⅰ的实验操作中,有将固体与液体分离过程即过滤操作,玻璃棒的作用是引流;
(2)步骤Ⅱ中发生的化学反应是锌与稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为:Zn+H2SO4=H2↑+ZnSO4;
(3)锌能置换出银,说明锌的活动性大于银,锌能与硫酸反应,银不能与硫酸反应,说明锌的活动性大于氢,氢大于银。由上述实验可得出锌、银、氢由强到弱的活动顺序为ZnHAg;
(4)锌与硫酸反应生成硫酸锌和氢气,氧化锌与硫酸反应生成硫酸锌和水,氢氧化锌与硫酸反应生成硫酸锌和水,碳酸锌与硫酸反应生成硫酸锌、二氧化碳和水。溶液D为硫酸锌和硫酸的混合溶液。若往溶液D中加入足量某物质,可得到只含一种溶质的溶液,则该物质可能是ABCD 。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目