题目内容
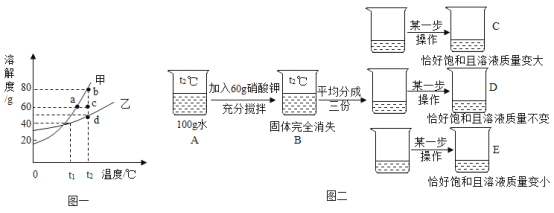
【题目】甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )
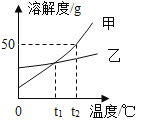
A.甲的溶解度大于乙的溶解度
B.t1℃时,甲、乙饱和溶液的溶质质量分数相等
C.将t2℃甲乙饱和溶液分别降温到t1℃,甲析出晶体,乙变成不饱和溶液
D.t2℃时,100g甲饱和溶液中含有50g甲
【答案】B
【解析】
A、溶解度比较,应指明温度,不然无法比较,不符合题意;
B、 t1℃时,甲、乙的溶解度相等,故甲、乙饱和溶液的溶质质量分数相等,符合题意;
C、甲、乙的溶解度都随温度的升高而增加,故将t2℃甲乙饱和溶液分别降温到t1℃,甲、乙均会析出固体,不符合题意;
D、t2℃时,甲的溶解度为50g,说明在100g溶剂中最多能溶解50g甲,不是100g溶液,不符合题意。
故选B。

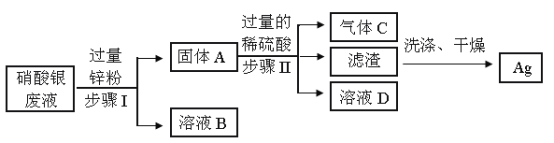
【题目】小明发现工业运输浓硫酸使用的是铁罐车,于是进行了探究。
(实验回顾)
把光洁的铁钉放到稀硫酸中,有气泡产生,请写出反应的化学方程式_____。
(提出问题)铁能与浓硫酸发生反应吗?为什么能用铁罐车来运输浓硫酸呢?
(查阅资料)
①常温下,铁与浓硫酸反应表面生成一层致密的氧化物薄膜,这层薄膜阻止了酸与内层金 属的进一步反应,化学上称之为钝化。
②SO2 可使品红溶液的红色褪去。
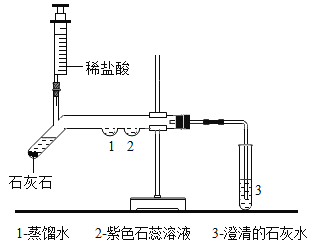
(实验探究)小明用相同的铁片和等量的浓硫酸按图 1 和图 2 所示的装置进行实验。
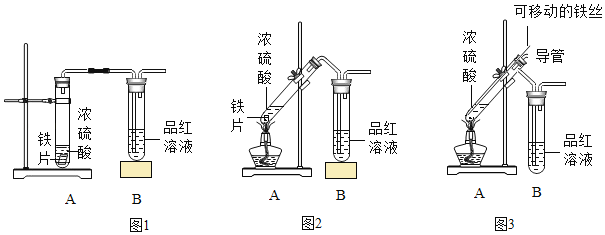
请帮助小明完成下表:
A 中硫酸浓度 | 实验条件 | B 中实验现象 | A 中生成的气体 | |
实验一 | 98% | 常温 | 品红溶液几乎不褪色 | 生成极少量的 SO2 |
实验二 | 98% | 加热 | 品红溶液褪色 | ______ |
(交流与讨论)
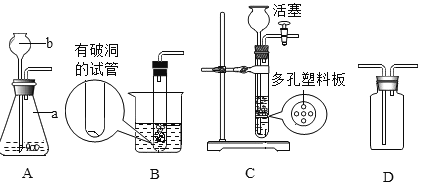
(1)小明将 A 装置进行了如图 3 所示的改进。 试分析用可移动的铁丝代替铁片的优点(至少写出两条)_____、_____。增加的导管有两个主要作用:一是在反应过程中,导 管伸入液面以下,起到液封作用,防止二氧化硫逸出;二是_____。
(2)在实验过程中,小明发现图 2 的装置有一处明显的不足,请对图 2 的装置提出改进意见_____。
(实验结论)铁与浓硫酸在加热条件下能持续反应,而常温下会因为钝化而使反应停止,
所以能用铁罐车运输冷的浓硫酸。
(实验反思)
(1)在加热的条件下铁与浓硫酸反应除生成二氧化硫外,还能生成硫酸铁和水。请写出铁与浓硫酸反应的化学方程式_____;
(2)经钝化处理后的铁丝在空气中不易生锈,原因是_____。