题目内容
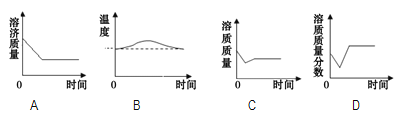
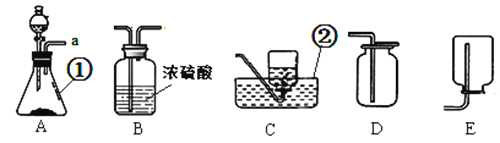
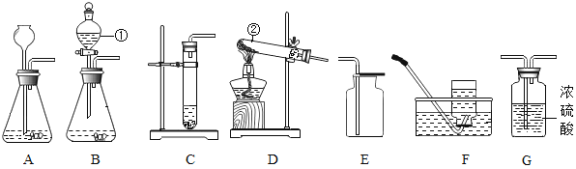
【题目】从宏观、微观和量的角度描述化学反应是化学特有的方式。下面是对稀盐酸与氢氧化钠反应的不同描述。图A是实际操作图,图B是微观粒子结合过程的图示,图C是反应过程中溶液的酸碱度变化曲线。根据要求回答下列问题:

(1)该变化对应的实验操作是将_______滴加到另一种溶液中;
(2)当滴入溶液的质量为ag时,溶液中溶质为______(填化学式);
(3)b点溶液中主要的离子是_____(填离子符号);
(4)该反应的实质是______
【答案】稀盐酸 NaOH、NaCl Na+、Cl- H++OH-=H2O
【解析】
(1)图C中pH是逐渐减小的,因此是把稀盐酸滴入氢氧化钠溶液中;
(2)当滴入溶液的质量为ag时,溶液的pH>7,氢氧化钠过量,溶液中的溶质为氯化钠和氢氧化钠,化学式为:NaOH、NaCl;
(3)b点溶液pH=7,当溶液的pH=7时,氢氧化钠和盐酸恰好完全反应,溶液中的主要离子是钠离子和氯离子,化学式为:Na+、Cl-;
(4)中和反应的实质是氢离子和氢氧根离子反应生成水的过程,表示为:H++OH-=H2O。

练习册系列答案
相关题目