题目内容
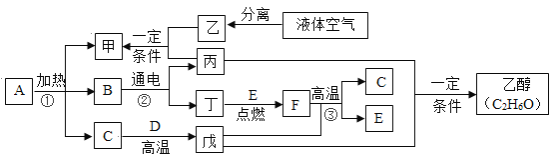
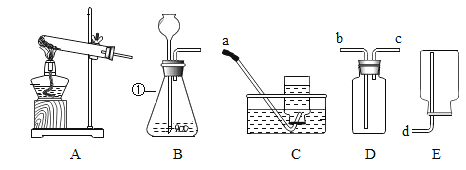
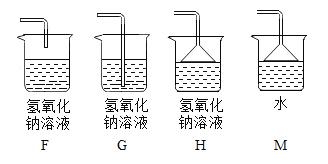
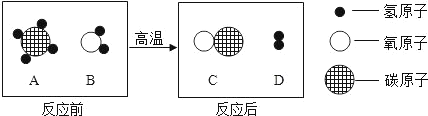
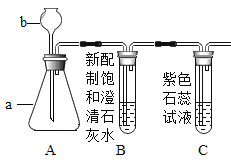
【题目】如下图是甲、乙、丙三个实验的示意图,根据图中所发生的反应现象及反应原理,进行总结归纳并回答下列问题:
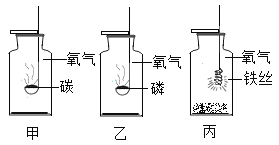
(1)所发生的三个反应有多个共同的特点,分别是:(只写四个即可)
①________________。
②________________。
③_________________。
④________________。
(2)甲实验进行的,燃烧匙中碳的状态是_______
(3)任选上述三个实验中的一个,写出反应的化学方程式:______
【答案】都是化合反应 都是物质 与氧气发生的反应 生成物均为氧化物 反应均放出大量的热(答案合理即可) 固态 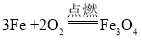
【解析】
图是甲、乙、丙三个实验的示意图分别是碳、磷和铁在氧气中燃烧,对比分析反应原理。
(1)这三个反应的共同特点分别是:
① 都是化合反应;
② 都是物质与氧气发生的反应;
③ 生成物均为氧化物;
④ 反应均放出大量的热。
(2)甲实验是碳燃烧,碳的熔点比较高,在燃烧进行进,燃烧匙中碳的状态是固态。
(3)上述三个实验中选择铁丝燃烧的反应,反应化学方程式为: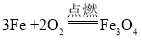

 天天向上一本好卷系列答案
天天向上一本好卷系列答案【题目】下列实验方法能达到实验目的的是( )
选项 | 实验目的 | 实验方法 |
A | 除去 | 加入足量锌粉 |
B | 检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
C | 检验蜡烛燃烧的产物中是否有水 | 在火焰上方罩一只冷而干燥的烧杯 |
D | 分离铜粉和铁粉 | 加水,过滤 |
A. A B. B C. C D. D
【题目】化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。
(1)请写出镁条燃烧的化学方程式__________。
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量。有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是:_________。
(3)小红按如图装置改进实验验证了质量守恒定律,还发现产物中有少量黄色固体。
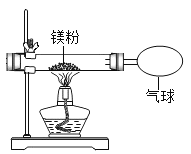
(提出问题)黄色固体是什么?
(查阅资料)①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(![]() )固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
(做出猜想)黄色固体是![]()
(实验探究)请设计实验,验证猜想
实验操作 | 实验现象及结论 |
____________ | ________________ |
(反思与交流)①空气中![]() 的含量远大于
的含量远大于![]() 的含量,可是镁条在空气中燃烧产物MgO却远多于
的含量,可是镁条在空气中燃烧产物MgO却远多于![]() ,合理的解释是:_________;
,合理的解释是:_________;
②同学们又联想到氢气在氯气中能够燃烧,于是对燃烧条件又有了新的认识:_________。