题目内容
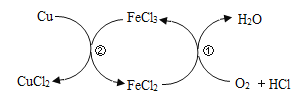
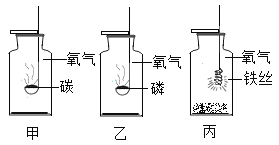
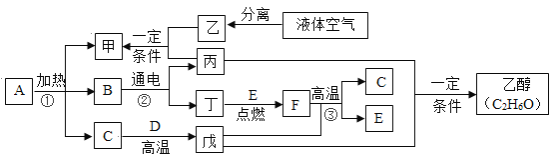
【题目】如图为某些物质间的转化关系,甲、乙、丙、丁、戊均为气体,甲有刺激性气味,乙是空气中含量最多的气体,戊有毒,D是黑色固体,E是应用最广泛的金属。部分生成物已略去。
(1)化学式:A__________.,乙___________。
(2)反应②、③的化学方程式:②_________;③____________.。
(3)液态空气中首先分离出乙,是利用乙的___________较低(选填“熔点”或“沸点”)。
(4)工业上可用丙和戊合成乙醇和B,反应中丙和戊的质量比为_____________。
【答案】NH4HCO3 N2 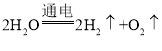
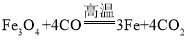 沸点 1:7
沸点 1:7
【解析】
乙是空气中含量最多的气体,推测乙是氮气;戊有毒,且为气体,推测戊为一氧化碳;B通电产生丙和丁,推测B为水;而丙能和氮气生成有刺激性气味的气体甲,则丙是氢气,和氮气生成氨气,则甲为氨气,丁则为氧气;E是使用最广泛的金属,则E是铁;氧气和铁反应生成F,则F是四氧化三铁;四氧化三铁和一氧化碳反应生成C和铁,则C是二氧化碳;二氧化碳和黑色固体D在高温下生成一氧化碳,则D是碳;A加热生成氨气、水和二氧化碳,推测A为碳酸氢铵。代入关系式可知推理正确。
(1)A为碳酸氢铵,化学式为NH4HCO3;乙为氮气,化学式为N2;
(2)反应②为水电解生成氢气和氧气,反应的化学方程式为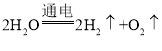 ;
;
反应③为四氧化三铁和一氧化碳反应生成铁和二氧化碳,反应的化学方程式为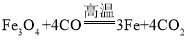 ;
;
(3)液态空气中首先分离出乙,是利用乙的沸点较低;
(4)工业上可用丙:氢气和戊:一氧化碳合成乙醇和B:水,反应的化学方程式为 ,则氢气和一氧化碳的质量比为(4×2):(2×28)=1:7。
,则氢气和一氧化碳的质量比为(4×2):(2×28)=1:7。

 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案【题目】日常生活中,每位同学都会接触到硬水。某化学兴趣小组同学对硬水进行了些探究实验,请完成填空(序数标号处)。
(查阅资料)水的硬度是由水中溶解的可溶性钙和镁化合物引起的。
(1)日常生活中常用煮沸的方法将硬水软化,这种方法可靠吗?小组同学设计了如下实验。
序号 | 实验操作 | 实验现象 |
Ⅰ | 分别取适量碳酸氢钙溶液于A、B两支试管中,加热A试管,B试管不加热。 | A试管中产生气泡,有沉淀生成,B试管中无明显现象。 |
Ⅱ | A试管冷却后,在上述两支试管中,分别滴加几滴肥皂水,振荡。 | _____(填“A”或“B”)试管中有较多泡沫,另一支试管中泡沫较少。 |
实验结论是:________。
(2)小组同学对某硬水中为什么含有碳酸氢钙非常感兴趣,在学习九年级化学上册课本中的“溶洞的形成”后知道:当石灰岩遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙:![]() 。小组同学向碳酸钠溶液中通入一定量的二氧化碳,所得溶液的溶质是什么?于是他们对此开展实验探究(不考虑二氧化碳和碳酸作为溶质的情况)
。小组同学向碳酸钠溶液中通入一定量的二氧化碳,所得溶液的溶质是什么?于是他们对此开展实验探究(不考虑二氧化碳和碳酸作为溶质的情况)
(提出猜想)猜想一:溶质为Na2CO3;猜想二:溶质为 NaHCO3;猜想三:溶质为______。
(设计实验)
实验步骤 | 实验现象 | 实验结论 |
a.取碳酸钠溶液通入一定量二氧化碳后所得的溶液少许于试管中,向其中滴加过量的CaCl2溶液 | 有白色沉淀生成 | 猜想二_____(填“成立”或“不成立”) |
b.取实验步骤a试管中的上层清液,滴加适量稀盐酸 | 有气泡冒出 | ______不成立 |
写出实验步骤a中发生反应的化学方程式______________。
通过实验,小组同学得出了正确结论。
(拓展延伸)将8.0g NaOH固体溶解在100mL水中,通入6.6g二氧化碳气体,充分反应后,所得溶液中溶质 NaHCO3的质量为___________。