题目内容
【题目】A、B、C三种固体物质的溶解度曲线如图所示,回答下列问题:
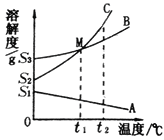
(1)图中M点的意义是_____。
(2)在0℃时,将B的l00g饱和溶液蒸发掉l0g水,再恢复到0℃,剩余溶液的质量为_____g。
(3)将0℃时物质C的饱和溶液升温至t2℃(溶剂不变),此时,其溶液的溶质质量分数为_____。
(4)已知C是一种白色固体,要使一杯不饱和的C溶液变成饱和溶液,可采取的一种方法是_____。
【答案】t1℃时,B、C溶解度相同 90-0.1S3 ![]() ×100% 蒸发溶剂,或加溶质或降温
×100% 蒸发溶剂,或加溶质或降温
【解析】
(1)由溶解度曲线可知:M点的意义是:t1℃时,B、C溶解度相同;
(2)设:在0℃时,将B的l00g饱和溶液蒸发掉l0g水,再恢复到0℃,析出的晶体质量为x。则有:![]() x=0.1S3g。在0℃时,将B的l00g饱和溶液蒸发掉l0g水,再恢复到0℃,剩余溶液的质量=100g-10g-0.1S3g= (90-0.1S3)g;
x=0.1S3g。在0℃时,将B的l00g饱和溶液蒸发掉l0g水,再恢复到0℃,剩余溶液的质量=100g-10g-0.1S3g= (90-0.1S3)g;
(3)0℃时物质C的饱和溶液的溶质质量分数=![]() ,C的溶解度随着温度的升高而增大,将0℃时物质C的饱和溶液升温至t2℃(溶剂不变),没有溶质析出,溶质的质量分数不变,此时其溶液的溶质质量分数=
,C的溶解度随着温度的升高而增大,将0℃时物质C的饱和溶液升温至t2℃(溶剂不变),没有溶质析出,溶质的质量分数不变,此时其溶液的溶质质量分数=![]()
(4)C的溶解度随着温度的升高而增大,要使一杯不饱和的C溶液变成饱和溶液,可采取的一种方法是蒸发溶剂或加溶质或降温。

练习册系列答案
相关题目