题目内容
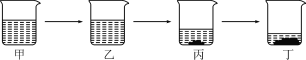
【题目】室温下,将甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙固体有剩余,乙固体全部溶解.升温至80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.图2可表示甲、乙、丙三种物质的溶解度曲线.
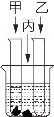
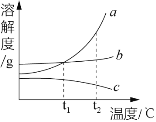
图1 图2
(1)图2中能表示乙物质的溶解度曲线的是__________(选填“a”、“b”或“c”).
(2)若丙中含有少量甲,可用___________法提纯丙.
(3)t2℃时,甲、乙、丙三种物质的等质量的饱和溶液中溶剂质量由大到小的顺序为_____.
(4)在温度__________时,甲物质的饱和溶液一定比丙物质的饱和溶液溶质质量分数更大.
【答案】c 蒸发结晶 c>b>a 80℃
【解析】
(1)如图1所示,甲、丙固体有剩余,乙固体全部溶解.升温至80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化,说明乙固体的溶解度随温度的升高而减小,所以图2中能表示乙物质的溶解度曲线的是c,故填c。
(2)如图1所示,丙固体有剩余。升温至80℃时,丙固体没有明显变化,说明丙的溶解度受温度影响变化不大,因此若丙中含有少量甲可用蒸发结晶法提纯丙,故填蒸发结晶。
(3)t2℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是a>b>c,所以t2℃时,甲、乙、丙三种物质的等质量的饱和溶液中溶剂质量由大到小的顺序为c>b>a,故填c>b>a。
(4)由题意知,升温至80℃时,甲固体全部溶解,丙固体的溶解量变化不大,所以在80℃时甲物质的饱和溶液一定比丙物质的饱和溶液溶质质量分数更大,故填80℃。

 阅读快车系列答案
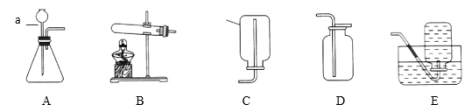
阅读快车系列答案【题目】下图所示为实验室中常见的气体制备和收集装置。
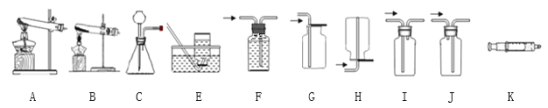
(1)实验室用高锰酸钾制取氧气,应选用发生装置_________(填字母序号,下空相同),收集装置可以选择__________,反应的文字表达为_______。
(2)注射器K可用于检查装置C的气密性,步骤如下:
①向锥形瓶中加入水至___________处。
②将注射器K连接到装置C的导管口处。
③缓慢拉动注射器K的活塞,观察到_______,表示装置C的气密性良好。
(3)为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
收集方法 | 向上排空气法 | 排水法 | ||||
氧气浓度% | 79.6 | 79.7 | 79.9 | 90.0 | 89.8 | 89.3 |
氧气平均浓度% | 79.7 | 89.7 | ||||
①用向上排空气法收集氧气时,以__________为氧气集满标准;
用排水法收集氧气时,以观察到_________为氧气集满的标准。
②以上两种方法中,______________法收集到的氧气更纯净。
③向上排空气法收集到的氧气浓度只有80%左右的原因有_________。
A.氧气的密度略大于空气的密度
B.加热高锰酸钾固体产生氧气的浓度只有80%左右
C.当观察到带火星木条复燃时,集气瓶内还有空气
D.当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
【题目】“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500 g溶质质量分数为0.9%的生理盐水,需要氯化钠固体____g。
下列实验操作与目的分析均正确的一组是________(填序号)。
项目 | 实验操作 | 目的分析 |
A | 称量时,将取出的过量氯化钠放回原瓶 | 节约药品 |
B | 溶解氯化钠时用玻璃棒搅拌 | 增大氯化钠的溶解度 |
C | 称取氯化钠时,在天平两边托盘上应当放一张质量相等的纸 | 整洁美观 |
D | 量取所需水时,视线与量筒液体凹液面的最低处保持水平 | 准确无误 |
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有:烧杯、玻璃棒、量筒和______。
(3)实验室若用恒温蒸发的方法将15%的氯化钠溶液变成饱和溶液,其过程如下图所示。与丙烧杯中溶液溶质质量分数一定相同的是______烧杯中的溶液。(填序号)