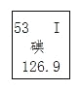
题目内容
【题目】实验室常用下列装置制取气体,请你根据所学知识回答下列问题:
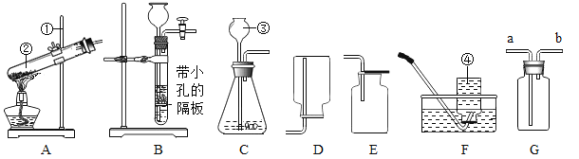
(1)写出编号所指仪器的名称:①_________;③____________。
(2)以上装置图中共有两处明显的错误,请你找出错误的地方并把改正的结果填在下列横线上:①_____________;②____________。
上述装置改进后,请继续回答下列问题。
(3)小李在实验室中用氯酸钾和二氧化锰制取纯净的氧气,化学方程式:________,他选择上述装置中的_______和________(填字母)进行组装。小红在实验室中选用C装置作为氧气的发生装置。请你写出小红制取氧气的化学反应方程式_______。
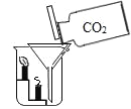
(4)实验室选用C和E装置还可以制取二氧化碳,需要的药品是______ (填名称),写出实验室制取该气体的化学方程式________。某同学将收集的二氧化碳气体向漏斗中倾倒观察的现象是______,由此说明二氧化碳具有的性质是________。实验室中检验二氧化碳气体的化学方程式为_______
(5)装置B、C都可以用来制取(4)中的气体,比较这两个装置的不同,指出B装置的一个突出优点___________。
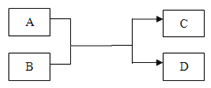
(6)有一名同学欲用G装置收集H2,则H2应从导管口______通入。
【答案】铁架台 长颈漏斗 试管口向上倾斜,应略向下倾斜 导气管没伸入集气瓶底,应伸入集气瓶底 2KClO3![]() 2KCl+3O2↑ A F 2H2O2
2KCl+3O2↑ A F 2H2O2![]() 2H2O+O2↑ 石灰石或大理石和稀盐酸 CaCO3+2HCl=CaCl2+H2O+CO2↑ 蜡烛由下向上依次熄灭 二氧化碳密度大于空气的密度,二氧化碳不可燃,也不支持一般可燃物燃烧 Ca(OH)2+CO2=CaCO3↓+H2O 可以控制反应的发生和停止 b
2H2O+O2↑ 石灰石或大理石和稀盐酸 CaCO3+2HCl=CaCl2+H2O+CO2↑ 蜡烛由下向上依次熄灭 二氧化碳密度大于空气的密度,二氧化碳不可燃,也不支持一般可燃物燃烧 Ca(OH)2+CO2=CaCO3↓+H2O 可以控制反应的发生和停止 b
【解析】
(1)编号①所指仪器的名称是铁架台;编号③所指仪器的名称是长颈漏斗;
(2)在以上装置中,A装置的试管口没有略向下倾斜,会导致生成的冷凝水回流,从而炸裂试管;E装置中导管太短,没有伸入集气瓶底,会造成收集的气体不纯。装置图中共有两处明显的错误分别是试管口向上倾斜,应略向下倾斜;导气管没伸入集气瓶底,应伸入集气瓶底;
(3)在二氧化锰催化作用下,氯酸钾加热时分解生成氯化钾和氧气,化学反应方程式为:2KClO3 ![]() 2KCl+3O2↑;用氯酸钾和二氧化锰制取氧气时,反应物的状态是固体,反应条件是加热,可选用发生装置A,氧气不易溶于水,排水法收集的氧气比较纯净,可选用的收集装置是F,故他选择上述装置中的A和F进行组装;小红在实验室中选用C装置作为氧气的发生装置,是固—液常温型反应,使用的药品是过氧化氢和二氧化锰,过氧化氢在二氧化锰催化作用下分解生成水和氧气;反应的化学方程式为:2H2O2
2KCl+3O2↑;用氯酸钾和二氧化锰制取氧气时,反应物的状态是固体,反应条件是加热,可选用发生装置A,氧气不易溶于水,排水法收集的氧气比较纯净,可选用的收集装置是F,故他选择上述装置中的A和F进行组装;小红在实验室中选用C装置作为氧气的发生装置,是固—液常温型反应,使用的药品是过氧化氢和二氧化锰,过氧化氢在二氧化锰催化作用下分解生成水和氧气;反应的化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(4)实验室选用C和E装置制取气体时反应物必须是固体和液体不需加热型,向上排空气法收集,说明该气体密度比空气大,二氧化碳适合这两点,制取时反应物为碳酸钙和稀盐酸,生成物是氯化钙、二氧化碳、水,反应的化学方程式为:CaCO3 +2HCl =CaCl2 + H2O + CO2↑;某同学将收集的二氧化碳气体向漏斗中倾倒观察的现象是蜡烛由下向上依次熄灭;由此说明二氧化碳具有的性质是二氧化碳密度大于空气的密度,二氧化碳不可燃,也不支持一般可燃物燃烧;二氧化碳与氢氧化钙反应生成碳酸钙和水。二氧化碳能使澄清石灰水变浑浊,常用于检验二氧化碳。实验室中检验二氧化碳气体的化学方程式为:Ca(OH)2 + CO2 = CaCO3 ↓+ H2O;
(5)在装置B中,固体药品物放在多孔隔板上,液体药品从长颈漏斗中加入。关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。B装置的一个突出优点是可以随时控制反应的发生与停止;
(6)氢气的密度小于空气,欲用G装置收集H2,则H2应从导管口b通入。

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案【题目】为探究影响大理石与稀盐酸反应剧烈程度的因素,某学习小组进行了探究。
(提出问题)影响大理石与稀盐酸反应剧烈程度的因素有哪些?
(猜想与假设)甲同学:__________
丙同学:溶液温度; 乙同学:酸的浓度。
(设计实验)小组同学将稀盐酸分成四等份,分别加入四支试管中进行下列对比实验。
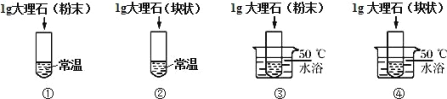
(实验验证)写出大理石与稀盐酸反应化学方程式:___________; 比较下表是同学进行的探究记录,请完善表格。
实验目的 | 对照组 | 实验现象 | 实验结论 |
探究温度对于反 应速率的影响 | ①和___________。 | ___________ | 温度越高化学反应应 速率越快 |
___________ | ③和④ | 实验③产生气泡速率比实验④快 | ___________ |