题目内容
【题目】教师设计如下实验帮助学生探究碳酸钠溶液中滴入稀盐酸的反应情况:
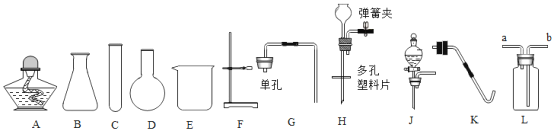
实验仪器: 60mL分液漏斗(有体积刻度的)、250mL广口瓶、磁力搅拌器。
实验试剂: Na2CO3 溶液(100.0mL 溶液中含有10.6g Na2CO3)、酚酞试液、稀盐酸(100.0mL 溶液中含有3.65g HCl)。
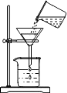
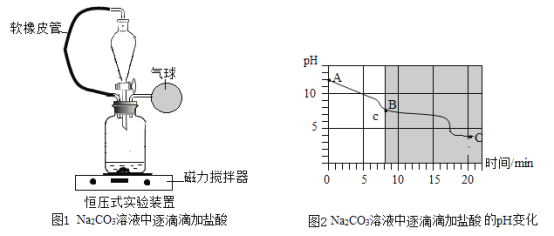
实验装置:如图1所示。
教师提示:
①酚酞试液变色范围: pH>10,显红色;10>pH>8.2,显粉红色; pH<8.2,显无色。
②本实验条件下,Na2CO3溶液pH约为12.0 ;NaHCO3溶液的pH约为8.5。
实验一:往碳酸钠溶液中逐滴滴大稀盐酸(如图1所示)
实验操作过程:
①检查装置的气密性后;在广口瓶中加入20.0mL Na2CO3溶液,再滴大几滴酚酞试液,在分液漏斗中加入40.0mL稀盐酸。
②打开磁力搅拌器,搅拌待反应溶液。然后打开分液漏斗活塞,逐滴滴入20.0mL稀盐酸,关闭活塞。观察到的现象:溶液由红色变成粉红色,反应没有气泡产生,气球没有增大。
③再次打开分液漏斗活塞,逐滴滴入剩余的20.0mL稀盐酸。
观察到的现象:溶液由粉红色变成无色,反应产生大量气泡,气球逐渐增大。
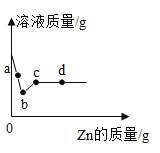
实验二:用数字化实验技术测定上述实验过程中pH的变化情况(如图2所示)
请回答下列问题:
(1)检查装置(如图1所示)的气密性的方法是:____________________________。
(2)磁力搅拌器的作用是__________________________。
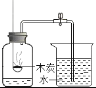
(3)气球的作用是__________________________。
(4)写出实验操作②结束后溶液(图 2中的B点)中所含溶质的化学式:__________________________。
(5)写出实验操作③中反应的化学方程式:__________________________。
(6)实验过程中产生的CO2质量为_________________________g。
【答案】用手(或热毛巾)捂住广口瓶,观察气球是否变大 使反应物能与稀盐酸及时并充分反应 缓冲瓶内气压的变化,观察反应过程中是否有气体产生 NaHCO3、NaCl ![]() 0.88
0.88
【解析】
(1)检查装置(如图1所示)的气密性的方法是:用手(或热毛巾)捂住广口瓶,观察气球是否变大,若气球变大,则装置气密性良好。故填:用手(或热毛巾)捂住广口瓶,观察气球是否变大;
(2)磁力搅拌器的作用是:使反应物能与稀盐酸及时并充分反应。故填:使反应物能与稀盐酸及时并充分反应;
(3)气球的作用是:缓冲瓶内气压的变化,观察反应过程中是否有气体产生。故填:缓冲瓶内气压的变化,观察反应过程中是否有气体产生;
(4)实验操作②结束后溶液变成粉红色(图2中的B点),此时碳酸钠和稀盐酸反应生成碳酸氢钠,溶液中所含溶质由碳酸氢钠和氯化钠。故填:NaHCO3、NaCl;
(5)实验操作③中,碳酸氢钠和稀盐酸反应生成氯化钠、二氧化碳和水,反应的化学方程式: ![]() 。故填:
。故填:![]() ;
;
(6) 100.0mL溶液中含有10.6g Na2CO3,20mL溶液中含有碳酸钠的质量为:10.6g×![]() =2.12g
=2.12g
设实验过程中产生的CO2质量为x。

x=0.88g
故填:0.88g。

【题目】下表列出了1 ~18号元素的原子序数和元素符号:
原子序数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
元素符号 | H | He | Li | Be | B | C | N | O | F |
原子序数 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
元素符号 | Ne | Na | Mg | Al | Si | P | S | Cl | Ar |
请回答下列问题:
(1)1 ~18号元素中属于稀有气体元素的有He、Ne、_____________ (填元素符号)。
(2)1 ~18号元素中最外层有2个电子的原子有____________、Be、Mg(填元素符号)。
(3)某元素的原子结构示意图为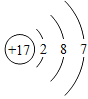 ,它在化学反应中一般易______________电子(填“得到”或“失去”),它与地壳中含量最多的金属元素形成化合物的化学式为_______________;它与11号元素组成的物质是由__________;构成的(填“分子”、“原子”或“离子”)。
,它在化学反应中一般易______________电子(填“得到”或“失去”),它与地壳中含量最多的金属元素形成化合物的化学式为_______________;它与11号元素组成的物质是由__________;构成的(填“分子”、“原子”或“离子”)。
(4)科学家已经研究出7号元素对应的高能微粒N5+,每个N5+中含有______________个质子和____________个电子。
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是____________(单选,填字母序号)
A NO和O2
B CO和N2
C SO2和CO2
D SO2和SO3
【题目】化学实验技能是学习化学和进行探究活动的基础和保证。以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究:
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等;猜想2:_____。
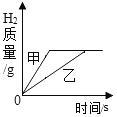
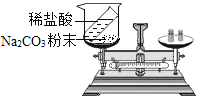
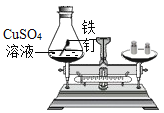
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生,天平指针向右偏转 | 铁钉表面有红色物质析出,溶液由蓝色变为浅绿色,天平指针没有偏转 |
结论 | 猜想1正确 | 猜想2正确,反应的化学方程式:_____ |
(反思与评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体逸出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在_____中进行。
(优化装置)同学们对甲组左盘中的反应装置进行了如下三种改进,查阅资料后发现最佳装置是B,则猜想B中氢氧化钠具有的化学性质是_____。
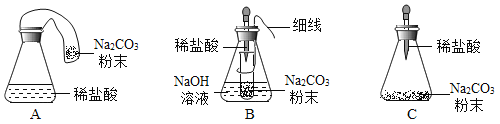
(得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。