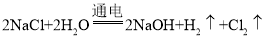题目内容
【题目】下列说法中正确的是
A.质量相等的氧化镁和硫酸镁中镁元素的质量比为1:3
B.质量相等的硫和碳分别在氧气中充分燃烧,硫比碳消耗氧气的质量大
C.硝酸铵和氯化钾混合物中氮元素质量分数为14%,该混合物中硝酸铵质量分数为40%
D.质量和质量分数均相等的氢氧化钠溶液和稀硫酸,充分反应后,向所得溶液中滴加紫色石蕊溶液,溶液呈蓝色
【答案】CD
【解析】
A、解:氧化镁和硫酸镁的质量都为m,质量相等的氧化镁和硫酸镁中镁元素的质量比为=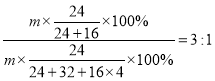 ;故选项错误;
;故选项错误;
B、解:设碳粉和硫粉的质量都为m,碳消耗的氧气质量为x,硫消耗的氧气质量为y
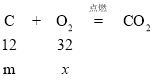
![]() x=
x=![]()
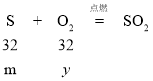
![]() y=
y=![]()
x>y;
质量相等的硫和碳分别在氧气中充分燃烧,碳比硫消耗氧气的质量大;故选项错误;
C、解:令混合物的质量为1,设混合物中硝酸铵的质量分数为x
一个硝酸铵分子中含有2个氮原子,则关系如下:
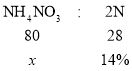
![]() x=40%
x=40%
该混合物中硝酸铵质量分数为40%;故选项正确;
D、由化学方程式可知:2NaOH+H2SO4=Na2SO4+2H2O,80份氢氧化钠与98份硫酸恰好完全反应,质量和质量分数均相等的氢氧化钠溶液和稀硫酸,充分反应后,氢氧化钠有剩余,溶液显碱性,向所得溶液中滴加紫色石蕊溶液,溶液呈蓝色;故选项正确;
故选:CD。

 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案【题目】U形管在实验中有广泛的应用。
实验一:探究分子的性质 | 实验二:验证氧化钙的性质 | 实验三: 探究金属的活动性强弱 | 实验四:实验室制取二氧化碳 |
|
|
|
|
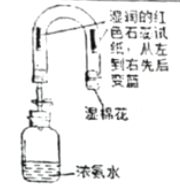
①实验一:说明分子具有的性质是_____________。
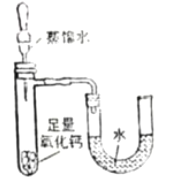
②实验二:观察到的现象是___________, 反应的化学方程式为_________。
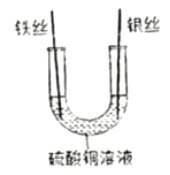
③实验三:能证明金属活动性Fe>Cu>Ag的现象是__________,反应一会儿后取出两种金属,溶液中溶质的存在情况是_________________。
④实验四:为了达到“随开随用,随关随停”的要求,装置的改进措施是___________________。