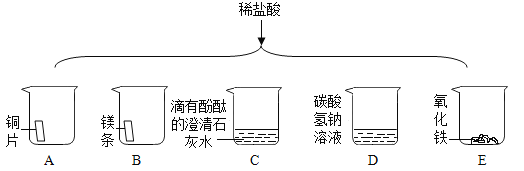
题目内容
【题目】实验室用纯净、干燥的的氢气还原氧化铜来测定水中氢元素和氧元素的质量之比(本实验制得的氢气中可能混有氯化氢和水蒸气)。设计如下实验装置:
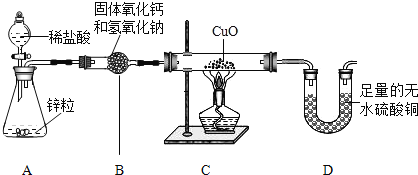
回答下列问题:
①实验开始时,应该先___________________(选填字母)。
a 给氧化铜加热 b 打开分液漏斗的活塞滴加酸液
②装置B的作用是___________________实验中若要验证氢气中混有氯化氢,该实验中改进的方法是___________________。若要避免有氯化氢气体产生,装置A中试剂应改成___________________溶液。
③装置C中的实验现象是___________________。
④反应后其数据如下表所示:
反应前 | 反应后 | |
(氧化铜+玻璃管)质量/g | 89.5 | 86.3 |
(硫酸铜+U 型管)质量/g | 214.4 | 218.0 |
根据实验数据填空,生成水中氢元素的质量为___________________克。
⑤上图中若没有装置B,并且不考虑空气中水分的影响,则测定结果中氢元素的质量会___________________(填“偏小”或“偏大”或“无影响”)。
【答案】b 除去氢气中可能含有的氯化氢气体和水蒸气 装置A和B之间连接一个装有硝酸银溶液的洗气瓶 稀硫酸 黑色粉末变成红色 0.4 偏大
【解析】
①实验开始时,应该先:打开分液漏斗的活塞滴加酸液产生氢气,将装置内的空气排除干净,防止后续实验发生危险;
②装置B中的氧化钙和氢氧化钠都是干燥剂,作用是:除去氢气中可能含有的氯化氢气体和水蒸气,实验中若要验证氢气中混有氯化氢,该实验中改进的方法是:装置A和B之间连接一个装有硝酸银溶液的洗气瓶,若溶液中有沉淀产生,则气体中混有氯化氢。若要避免有氯化氢气体产生,装置A中试剂应改成稀硫酸溶液。
③装置C中氢气与灼热的氧化铜反应产生铜,实验现象是:黑色粉末变成红色;
④反应前后(氧化铜+玻璃管)的质量差表示产生水中氧元素质量=89.5g-86.3g=3.2g;
反应前后(硫酸铜+U 型管)的质量差表示吸收水的质量=218.0g-214.4g=3.6g;
生成水中氢元素的质量为=3.6g-3.2g=0.4g;
⑤上图中若没有装置B,并且不考虑空气中水分的影响,装置A中部分水蒸气会进入D装置,导致D装置质量变化偏大,则测定结果中氢元素的质量会偏大。

 53随堂测系列答案
53随堂测系列答案【题目】重庆市农村贫困地区义务教育学生营养餐全覆盖,合理搭配饮食是营养改善计划的健康原则。下表为某校食堂某天午餐部分食谱:
主食 | 荤菜 | 素菜 | 饮料 |
米饭 | 红烧牛肉 | 炒胡萝卜、炒黄瓜 | 牛奶 |
(1)食谱中富含蛋白质的是____,富含维生素的是____(填一种主食、菜名或饮料)。健康青少年每天要摄入维生素C(Vc)最低需要量为60 mg,完全来自西红柿,若100 g西红柿含Vc 20 mg,则每天至少应食用____g西红柿。
(2)学校厨房用铁锅作炊具主要利用铁的_____性。同时还可补充人体所需的铁元素,如果铁元素摄入量过少会引起______。
(3)早餐面包采用发酵粉(含碳酸氢钠和有机酸等)与面粉、水混合制作,面包小孔中的无色气体是___(填化学式),烤制面包时碳酸氢钠受热分解的化学方程式为_____。
(4)炒菜时,燃气灶的火焰呈黄色,锅底出现黑色,此时可将灶具的进风口______(填“调大”或 “调小”);油锅中的油不慎着火,可用锅盖盖灭,其灭火原理是_____。
(5)餐具上的油污可用洗洁精来洗掉,这是利用洗洁精的___(填“溶解”或“乳化”)作用。
(6)某同学给学校食堂的下列建议不合理的是_____(填序号)。
A 在主食中补充粗粮 B 多提供油炸食物 C 适当提供水果