题目内容
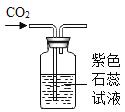
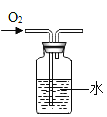
【题目】为了探究二氧化碳的性质,某同学设计了如图所示的实验:
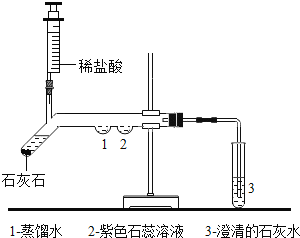
(1)写出石灰石与稀盐酸反应的化学方程式:___________________________________。
(2)用注射器注入稀盐酸,一段时间后,可观察到在1、2两处中有一处有明显的现象发生,该实验现象是______________________。
(3)3处的澄清石灰水变浑浊,这是由于________________________的缘故。
【答案】CaCO3+2HCl=CaCl2+H2O+CO2↑ 2处液体由紫色变成红色 二氧化碳与氢氧化钙反应,生成了白色的碳酸钙沉淀
【解析】
(1)石灰石与稀盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(2)二氧化碳的水溶液能使紫色石蕊变红,故2处中的紫色石蕊变红;
(3)3处的澄清石灰水变浑浊,原因是二氧化碳与石灰水中的氢氧化钙反应生成难溶于水的白色沉淀碳酸钙。

练习册系列答案
相关题目
【题目】某同学从定量角度研究双氧水制取氧气的过程,对原实验进行部分改进,增加了称量操作.具体做法是:取10%的双氧水和少量的二氧化锰放入气体发生装置,并对反应前后混合物的质量进行称量,记录如下:
反应过程 | 反应前 | 反应后 |
质量变化(不含容量质量) | 34.3g | 32.7g |
若反应后,双氧水分解完全且氧气全部逸出,该同学得出的结论中,不合理的是:
A.反应速率逐渐加快 B.最多得到氧气的质量为1.6g
C.催化剂二氧化锰的质量为0.3g D.反应得到水和氧气的质量比为9:8