题目内容
【题目】浴室喷头长时间使用会有白色固体附着,俗称水垢。这是因为硬水中含有较多的可溶性的碳酸氢钙【Ca(HCO3)2】,还含有可溶性的碳酸氢镁【Mg(HCO3)2】。查阅资料,加热时会产生难溶性的固体。其中碳酸氢钙【Ca(HCO3)2】受热易分解,生成难溶性的化合物、气体等物质。某小组想探究碳酸氢钙受热分解后产物的成分。
(1)【提出猜想】猜想1.难溶性化合物可能是CaCO3;猜想2.气体可能是H2、CO、CO2 。
【方案设计】请你设计实验,帮助该组同学确定难溶物的成分。
实验步骤 | 实验现象 | 结论 |
难溶物是CaCO3 |
(2)【实验探究】该组同学设计如图实验,继续探究气体的成分。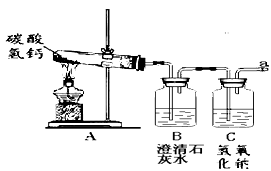
操作1.加热A装置,一段时间后,B装置中的澄清石灰水变浑浊。
操作2.在a处用燃着的木条检验,无明显现象。
【实验结论】结论1.碳酸氢钙分解产生的气体是;
结论2.碳酸氢钙受热分解的化学方程式为。
(3)【反思评价】有同学提出:硬水中可溶性的碳酸氢镁【Mg(HCO3)2】受热也会产生不溶性的固体,那水垢的成分中还有什么物质?根据上述探究,该组同学设计如下图装置进一步实验。(已知碱石灰主要成分为CaO和NaOH)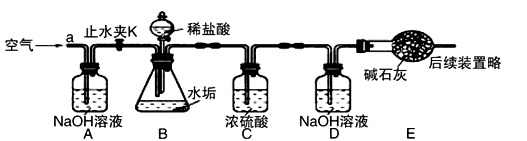
【实验测定】 步骤如下:
①按图组装仪器,先 , 再将50g水垢样品放入锥形瓶中。
②打开止水夹K,从导管a处缓缓鼓入一定量的空气。
③逐滴加入足量稀盐酸,待锥形瓶中出现气泡不再产生现象时,停止滴加稀盐酸。
④打开止水夹K,从导管a处缓缓鼓入一定量的空气;
⑤称量D瓶内物质增加的质量,直至D瓶内物质质量不变;
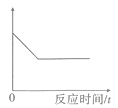
⑥测量滴加稀盐酸体积与D瓶内物质增加质量的关系如下图曲线所示。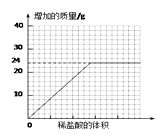
(4)【讨论交流】
①A装置中的NaOH溶液的作用是 , 若没有A装置,D装置中的质量将(填“偏大”、“不变”或“偏小”)。
②C装置中浓硫酸的作用是 , E装置的作用是。
③分析曲线图,通过计算可知:水垢中一定含有(化学式) , 理由是。
④查阅资料:水垢的主要成分有CaCO3、MgCO3和Mg(OH)2三种成分,三种物质加热后均能生成两种氧化物。小组同学提出探究水垢中氢氧化镁的质量分数:另取质量为50g的水垢试样,放入试管中加热至质量不再减少为止,测得二氧化碳24 g,残留固体25.1g。结合以上数据,确定水垢样品中氢氧化镁的质量分数为。(结果保留小数点后一位)
【答案】
(1)取样,滴加稀盐酸,有气泡产生
(2)CO2,Ca(HCO3)2 ![]() CaCO3 ↓+ CO2↑+H2O
CaCO3 ↓+ CO2↑+H2O
(3)检查装置气密性
(4)吸收鼓入空气中的二氧化碳,偏大,吸水干燥,吸收外界空气中CO2和H2O,MgCO3(或CaCO3和MgCO3),若只有CaCO3则50g只能生成CO222g,测定生成的CO224g,则一定还有MgCO3,5.8%
【解析】(1).碳酸盐能与酸反应生成二氧化碳,所以取样,滴加稀盐酸,有气泡产生,可证明难溶物是CaCO3;(2)碳酸氢钙分解产生气体CO2、碳酸钙、水;反应方程式为:Ca(HCO3)2 ![]() CaCO3↓+CO2↑+H2O;(3).做实验时要先检查装置气密性,然后再加入药品;(4).A装置中的NaOH溶液的作用是吸收鼓入空气中的二氧化碳,因二氧化碳和氢氧化钠反应生成碳酸钠和水;(7).若没有A装置,D装置将吸收空气中的二氧化碳,导致质量偏大(8).浓硫酸有吸水性,可吸水干燥二氧化碳;E装置的作用是吸收外界空气中CO2和H2O;D装置中的质量将吸收空气中的二氧化碳,导致质量偏大;水垢的成分是碳酸钙和氢氧化镁;每碳酸钙完全反应生成44g二氧化碳,每84g碳酸镁完全反应生成44g二氧化碳,因为若只有CaCO3则50g只能生成CO222g,测定生成的CO224g,则一定还有MgCO3;碳酸镁在加热条件分解生成氧化镁和二氧化碳,碳酸钙在加热条件下生成二氧化碳和氧化钙,氢氧化镁加热条件下分解生成氧化镁和水;所以加热后减少的是水的二氧化碳的总量;质量为50g的水垢试样,放入试管中加热至质量不再减少为止,残留固体25.1g,则生成二氧化碳和水的总量为:50g-25.1g=24.9g,测得二氧化碳24g,所以水的质量为0.9g。氢氧化镁可看做MgOH2O,氢氧化镁的质量为:0.9g÷(18÷58×100%)=2.9g;水垢样品中氢氧化镁的质量分数为2.9g÷50g×100%=5.8%。
CaCO3↓+CO2↑+H2O;(3).做实验时要先检查装置气密性,然后再加入药品;(4).A装置中的NaOH溶液的作用是吸收鼓入空气中的二氧化碳,因二氧化碳和氢氧化钠反应生成碳酸钠和水;(7).若没有A装置,D装置将吸收空气中的二氧化碳,导致质量偏大(8).浓硫酸有吸水性,可吸水干燥二氧化碳;E装置的作用是吸收外界空气中CO2和H2O;D装置中的质量将吸收空气中的二氧化碳,导致质量偏大;水垢的成分是碳酸钙和氢氧化镁;每碳酸钙完全反应生成44g二氧化碳,每84g碳酸镁完全反应生成44g二氧化碳,因为若只有CaCO3则50g只能生成CO222g,测定生成的CO224g,则一定还有MgCO3;碳酸镁在加热条件分解生成氧化镁和二氧化碳,碳酸钙在加热条件下生成二氧化碳和氧化钙,氢氧化镁加热条件下分解生成氧化镁和水;所以加热后减少的是水的二氧化碳的总量;质量为50g的水垢试样,放入试管中加热至质量不再减少为止,残留固体25.1g,则生成二氧化碳和水的总量为:50g-25.1g=24.9g,测得二氧化碳24g,所以水的质量为0.9g。氢氧化镁可看做MgOH2O,氢氧化镁的质量为:0.9g÷(18÷58×100%)=2.9g;水垢样品中氢氧化镁的质量分数为2.9g÷50g×100%=5.8%。
所以答案是:取样,滴加稀盐酸;有气泡产生;CO2;Ca(HCO3)2![]() CaCO3 ↓+ CO2↑+H2O;检查装置气密性;吸收鼓入空气中的二氧化碳;偏大;吸水干燥;吸收外界空气中CO2和H2O;MgCO3(或CaCO3和MgCO3);若只有CaCO3则50g只能生成CO222g,测定生成的CO224g,则一定还有MgCO3;5.8%。
CaCO3 ↓+ CO2↑+H2O;检查装置气密性;吸收鼓入空气中的二氧化碳;偏大;吸水干燥;吸收外界空气中CO2和H2O;MgCO3(或CaCO3和MgCO3);若只有CaCO3则50g只能生成CO222g,测定生成的CO224g,则一定还有MgCO3;5.8%。
【考点精析】通过灵活运用根据化学反应方程式的计算,掌握各物质间质量比=系数×相对分子质量之比即可以解答此题.

 阅读快车系列答案
阅读快车系列答案