题目内容
【题目】利用氢气(H2)和空气中分离出的氮气(N2)可以合成氨气(NH3),下列是合成氨的工艺流程图:
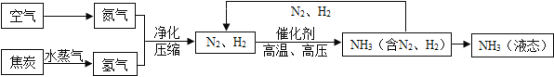
(1)根据下表中各物质的沸点,如要将产物 NH3 与 N2、H2 分离开来,温度应该控制在_____℃的范围之内。
物质 | H2 | N2 | NH3 |
沸点/℃ | -252 | -195.8 | -33.4 |
(2)用“〇”表示氢原子,“![]() ”表示氮原子,“
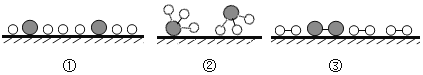
”表示氮原子,“![]() ”表示 催化剂,观察下列微观图,合成氨化学反应过程的微观顺序为_____(将下面三张图用序号排列)。
”表示 催化剂,观察下列微观图,合成氨化学反应过程的微观顺序为_____(将下面三张图用序号排列)。
(3)用焦炭(主要成分是碳)和水蒸气在高温条件下反应可制得氢气和另一种常温下为气态的有毒物 质,该反应的化学方程式:_____。 在煤和水蒸气反应前需先将煤粉碎,这样做的目的是_____。
(4)生产中 N2、H2 不可能全部转化为 NH3。将降温分离出的 N2、H2 送回合成塔目的是_____。
A充分利用原料 B防止氮气污染空气
【答案】-195.8~-33.4℃的 ③①② C+ H2O![]() H2+CO 增大反应物之间的接触面积,使反应充分快速 A
H2+CO 增大反应物之间的接触面积,使反应充分快速 A
【解析】
(1)如要将产物NH3与N2、H2分离开来,应将氢气和氮气进行蒸发,氨气不能蒸发,所以温度应该控制在-195.8~-33.4℃的范围之内。
(2)由化学反应的实质是分子的破裂原子的重新组合可知,合成氨化学反应过程的微观顺序为:③①②。
(3)用焦炭(主要成分是碳)和水蒸气在高温条件下反应可制得氢气和另一种常温下为气态的有毒物质,由质量守恒定律和物质的性质可知该物质是一氧化碳,该反应的化学方程式是:C+ H2O![]() H2+CO;
H2+CO;
在煤和水蒸气反应前需先将煤粉碎,这样做的目的是:增大反应物之间的接触面积,使反应充分快速。
(4)实际生产中,N2和H2不可能全部转化为NH3.将降温分离出的N2、H2送回合成塔的目的是充分利用原料。故填A。