题目内容
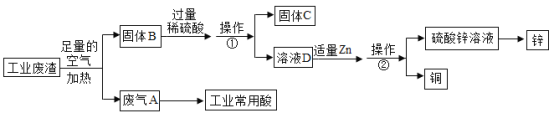
【题目】海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等。综合利用海水制备金属镁的流程如下图所示:
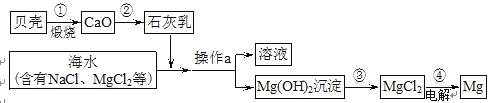
(1)贝壳主要成分的化学式是_________。
(2)操作a的名称是_______,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、_______。
(3)工业冶炼镁常用电解MgCl2的方法,反应为:MgCl2![]() Mg+_____。
Mg+_____。
(4)写出第②、③两步反应的化学方程式:
②___________________,③____________________。
【答案】CaCO3 过滤 漏斗 Cl2 CaO+H2O=Ca(OH)2 Mg(OH)2+2HCl=MgCl2+2H2O
【解析】
(1)贝壳的主要成分是碳酸钙(CaCO3)。
(2)石灰乳主要成分是氢氧化钙[Ca(OH)2],与海水中的氯化镁反应生成氢氧化镁[Mg(OH)2]沉淀和氯化钙溶液,应用过滤方法分离不溶性固体氢氧化镁和氯化钙溶液;过滤需要用烧杯、玻璃棒、漏斗等仪器。
(3)氯化镁电解生成镁和氯气(Cl2),则反应为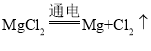 。
。
(4)第②步反应是氧化钙(CaO)与水化合生成氢氧化钙,第③步是氢氧化镁与盐酸反应生成氯化镁(MgCl2)和水,反应的化学方程式为②是CaO+H2O=Ca(OH)2,③是Mg(OH)2+2HCl=MgCl2+2H2O。

练习册系列答案
相关题目