题目内容
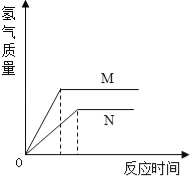
【题目】相同质量的M、N两种活泼金属,分别与足量质量分数为8%的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如图.下列叙述正确的是
A. 金属的活泼性N>M
B. 两个反应生成H2的体积相等
C. 相对原子质量N>M
D. 两个反应消耗盐酸的质量一定相等
【答案】C
【解析】A、根据图象可以看出,纵坐标表示氢气质量,横坐标表示时间,斜率表示反应的速度,M的斜率比N的大,所以M比N反应的速度快,所以M比N活泼,故A错误;
B、根据图象可以看出,M产生的氢气多,N产生的氢气少,两种金属产生的氢气质量不同,所以体积不同,故B错误;
C、M产生的氢气比N多,价态相同的金属与足量的酸反应,相对原子质量越大,产生的氢气越少,说明N的相对原子质量大,故C正确;
D、若两个反应消耗盐酸的质量,则置换出的氢的质量相等,产生的氢气的质量应该相同,而由图象可以看出,产生的氢气质量不相等,故D错误,
故选C.

练习册系列答案
相关题目