题目内容
【题目】蜡烛(足量)在如下左图密闭的集气瓶内燃烧至熄灭,用仪器测出瓶内氧气含量的变化如下右图所示。下列判断正确的是( )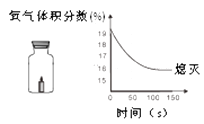
A.蜡烛燃烧前瓶内只有氧气
B.氧气浓度小于一定值时,蜡烛无法燃烧
C.过程中瓶内物质发生了化合反应
D.蜡烛熄灭后瓶内只剩二氧化碳气体
【答案】B
【解析】A、据图可知,蜡烛燃烧瓶前氧气的体积分数为20%左右,所以除了氧气之外还有其它气体,A不符合题意;
B、据图可知,当氧气体积分数达到16%左右,蜡烛熄灭,说明氧气浓度小于一定值时,蜡烛无法燃烧,B符合题意;
C、蜡烛燃烧是和氧气反应,生成二氧化碳和水,有两种新的物质,故过程中瓶内物质发生的不是化合反应,C不符合题意;
D、蜡烛熄灭后瓶内除了蜡烛燃烧生成的二氧化碳气体,还有原来瓶中含有的气体气体,D不符合题意;
所以答案是:B
【考点精析】本题主要考查了氧气的化学性质和化合反应及其应用的相关知识点,需要掌握氧气的化学性质:特有的性质:支持燃烧,供给呼吸;化合反应:由两种或两种以上物质生成另一种物质的反应才能正确解答此题.

【题目】某化学小组测定空气中氧气的体积分数。
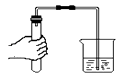
(1)根据下图回答问题。
①红磷燃烧的文字表达式为。
②红磷燃烧时的现象是 , 冷却到室温打开止水夹后,观察到的现象是烧杯中的水。
③冷却至室温后打开止水夹,发生上述现象的原因是。
④实验结论:
(2)用四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数。
反应原理为:2Na2S4+O2+2H2O =8S↓+4NaOH(氢氧化钠)。
小资料:四硫化钠(Na2S4)与氧气、水反应生成难溶于水的固体硫(S)和易溶于水的氢氧化钠。
【实验过程】
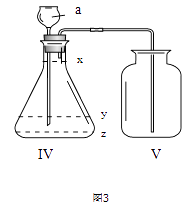
①取足量的四硫化钠固体加入试管中,再加入适量的水,迅速塞紧橡胶塞,充分振荡。测量液面至橡胶塞下沿的距离,记录数据h1(如图1所示)。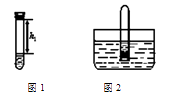
②将该试管插入水中(如图2所示),拔下橡胶塞,观察到 , 塞紧橡胶塞。将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2。理论上h2∶h1=。
③按照①和②再重复实验2次。3次实验数据如下表所示。
第1次 | 第2次 | 第3次 | |
h1/cm | 11.0 | 11.4 | 11.6 |
h2/cm | 8.7 | 9.1 | 9.2 |
根据第3次实验数据,计算空气中氧气的体积分数为%(结果精确到 0.1%)。