题目内容
【题目】铁、铝、铜是常见的三种金属。生活中的铝制品和铜器表面一般不用防锈,而铁制品则需防锈处理。
(提出问题)这三种金属的活动性强弱到底如何呢?
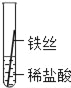
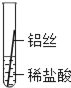
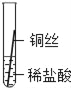
(实验探究)同学们将粗细相同的铁丝、铝丝、铜丝分别插入等体积、等浓度的稀盐酸溶液中:
操作 |
|
|
|
片刻后现象 | 缓慢产生少量气泡 | 无气泡 | 无气泡 |
几分钟后现象 | 缓慢产生少量气泡 | 快速产生大量气泡 | 无气泡 |
(讨论交流)
分析上述现象,得出三种金属的活动性由强到弱的顺序是_____。
铝丝插入稀盐酸的实验中,请你分析随着时间变化而出现的现象,并猜测该过程中还发生了什么反应?_____。(用文字叙述)
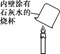
(反思改进)氧化铝与稀盐酸反应
做验证金属的性质实验前,需对金属进行怎样的处理?_____。
有同学提出“只用一支盛有少量稀盐酸的试管,只需调整金属丝的插入顺序,也能证明三种金属的活动性顺序”。则金属丝的插入顺序可以为_____(填一种顺序即可)。
(拓展迁移)将一定质量的铝粉放入含有硫酸亚铁、硫酸铜的混合溶液中,充分反应后,过滤。向滤出的固体中滴加稀硫酸,发现有气泡产生。
滤液中一定含有的溶质是_____(填化学式)。
该过程中产生气体时,一定发生的反应的方程式为_____。
【答案】Al>Fe>Cu 稀盐酸先与表面的氧化铝反应生成氯化铝和水,后与里面的铝反应生成氯化铝和氢气 除去金属表面的氧化层 Cu、Fe、Al Al2(SO4)3 Fe+H2S04=FeS04+H2↑
【解析】
讨论交流:对上述现象进行分析,三种金属的活动性由强到弱的顺序是 Al>Fe>Cu。
铝丝插入稀盐酸的实验中,随着时间的变化出现了开始没有气泡,后来产生气泡的现象,猜测该过程中还发生的反应为 Al2O3+6HCl=2AlCl3+3H2O。
反思改进:做验证金属的性质实验前,需对金属进行的处理为:打磨除锈,除去表面的氧化膜。
铜不能与盐酸反应,可先把铜放入稀盐酸,观察到无明显现象,说明铜位于氢之后;然后把铁放入该稀盐酸,铁与盐酸反应放出氢气,说明铁位于氢之前;待完全反应后,取出铁丝,插入铝丝,在铝丝表现出现黑色,说明铝的活动性比铁强。
故若只用一支盛有少量稀盐酸的试管,只需调整金属丝的插入顺序为Cu、Fe、Al,也能证明三种金属的活动性顺序。
拓展迁移:在金属活动性顺序中,铜、铝、铁、氢的活动性顺序为铝>铁>氢>铜。所以向FeSO4和CuSO4和稀硫酸混合溶液中投入一些铝粉,发生的反应依次有:铝与硫酸铜的反应,生成硫酸铝和铜;铝与硫酸反应生成硫酸铝和氢气,铝与硫酸亚铁的反应,生成硫酸铝和铁。由于向滤渣中加入少量稀盐酸,有气泡产生,说明滤渣中一定含有铁和铜,“可能”含有铝,则滤液中“一定”含有硫酸铝,可能含有硫酸亚铁,一定不含硫酸铜和稀硫酸。故将一定质量的铝粉放入含有硫酸亚铁、硫酸铜的混合溶液中,充分反应后,过滤。向滤出的固体中滴加稀硫酸有气泡产生。滤液中一定含有的金属化合物是硫酸铝。该过程中有气体生成时一定发生的反应的化学方程式 Fe+H2S04=FeS04+H2↑。

【题目】下列实验设计不能达到实验目的的是( )
选项 | A | B | C | D |
实验设计 |
|
|
|
|
实验目的 | 探究二氧化锰能否加快过氧化氢分解 | 探究石蜡燃烧后是否有二氧化碳生成 | 检验氧气是否集满 | 测定空气中氧气的含量 |
A. A B. B C. C D. D