��Ŀ����
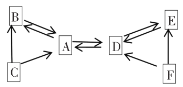
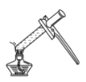
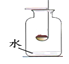
����Ŀ��(1)��֪��������Ҫ�ɷ��ǵ�����������ij����С����Ʋⶨ����������������ʵ�飬ʵ��װ����ͼ��ʾ������ȴ�����º���ɼк�۲쵽��ʵ������Ϊ_____����ʵ���к����Թ�����Ŀ����________��
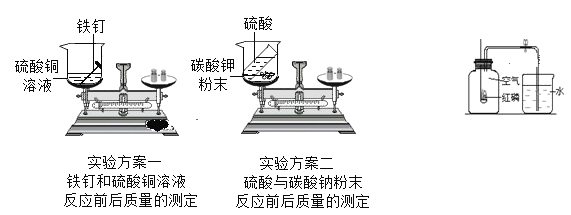
(2)�������ѧϰ�����������غ㶨������ʵ��̽��������Ҫ�����ʵ�鷽��һ��ʵ�鷽������(�±�����ʵ�������ѡ����=������>������<������)
ʵ�鷽�� | ����һ | ������ |
��Ӧ���� | �������渲��һ���ɫ�����ʣ���Һ����ɫ���dz��ɫ�� | _____________________�� |
��Ӧǰ�������� | m1 | n1 |
��Ӧ��������� | m2 | n2 |
ʵ����۷��� | m1______m2 | n1______n2 |
������ʵ�������жԱ�����ʱ����ͬѧ��һ�������۲쵽��ƽ��ƽ�⣬����Ϊ______����˲���˵�������غ㡣�ڷ�Ӧ�ﲻ���ǰ���£�Ҫʹ��ƽƽ�⣬��Ը÷����ĸĽ���ʩ��_____��
���𰸡��ձ��е�ˮ���뼯��ƿ�У�����ˮ�����Լռ����ƿ�ڿ��������![]() �ľ����� = �������������� > ���ɵ������ݳ� ���ܱյ������н���ʵ��
�ľ����� = �������������� > ���ɵ������ݳ� ���ܱյ������н���ʵ��
��������
(1)����ȼ����������������ƿ��������٣�ѹǿ��С���ڴ���ѹ�������£��ձ��е�ˮ���뼯��ƿ�ڣ����뼯��ƿ�ڵ�ˮ�����������������������������ĺ����ܺľ�������ʹʵ������ȷ��
(2)����һ������������ͭ��Һ��Ӧ����ͭ�������������˷�Ӧû�������ɣ����������ʵ��������䣬������ƽƽ�⣬���=��������������Ӧ����������̼���壬�����д������ݲ��������ڲ����Ķ�����̼��ɢ��������ȥ�ˣ������������������>����
�ڶ��������е�������Ϊ�������ݳ����������٣���ƽʧȥƽ�⣬���뿴����ƽƽ�⣬Ӧ���ܱ������н������飬���岻���ݳ���

 ���Ǽ���С����ϵ�д�
���Ǽ���С����ϵ�д� �Ͻ�ƽ���Ȿϵ�д�
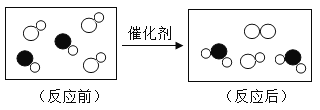
�Ͻ�ƽ���Ȿϵ�д�����Ŀ��������ʶ��ѧ��Ӧ���ܺ�����Ӧ����Ϊ��������밴Ҫ��ش�
��ѧ��Ӧ | ��Ӧ���� | ���ֱ���ʽ | �������� | ��;����һ���� |
������ؼ��ȷֽ� | ��______ | |||
ͭ˿�ڿ����м��� | ��______ | |||
þ��ȼ�� | ��______ | |||
��˿��������ȼ�� | ��______ |
����Ŀ����ͬѧ�Ժ�ʹ���ټ�����ơ���ʹ�֡����ķ���ԭ��������Ũ����Ȥ�����Ǵ��˼�����ʹ�֣�����ʵ���Ҷ�������о���

���������ϣ�
[ ԭ�ϲ� ] ������ʯ������̿��ˮ�ȡ�
[ ����ԭ�� ] ����������ˮ��Ӧ�����������������壩�������ȡ�
��ʵ�飩��֤��ʹ�ֳɷ����������Ļ�ѧ���ʡ�
���� | ʵ����� | ʵ������ |
����ʹ�ִ���ҩ�ﵹ��һ�ձ��У��۲� | ҩ��Ϊ��ɫ�����ĩ | |
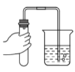
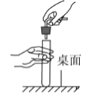
��һ���δ������ձ��еĺ�ɫ��ĩ��ֽӴ���ȡ���������ڴ����ϵĺ�ɫ��ĩ����ȼ�ճ��У��ھƾ����ϵ�ȼ������ʢ�������ļ���ƿ�У��۲졣
| ����ȼ�գ�_________ |
ʵ����ۣ�д���˷�Ӧ�Ļ�ѧ����ʽ________________��
����ƿ�м�ˮ��������_________________��