题目内容
【题目】家用纯碱样品中只含有少量的杂质氯化钠,某同学欲测定该样品中碳酸钠的含量。他取该纯碱样品 21.8 克,全部溶解在 100 克水中,再加入氯化钙溶液 98.2 克,恰好完全反应。过滤干燥 后称得沉淀质量为 20 克。请计算:
(1)纯碱样品中碳酸钠的质量。
(2)反应后所得滤液中溶质的质量分数。
【答案】(1)21.2g ,(2)12%
【解析】
由已知条件“再加入氯化钙溶液 98.2 克,恰好完全反应。过滤干燥 后称得沉淀质量为 20 克。”列出化学反应方程式,标出相应数值,可以计算出恰好完全反应时参加反应的碳酸钠的质量和反应生成的氯化钠质量,进而求解反应后所得滤液中溶质的质量分数。
(1)设恰好完全反应时参加反应的碳酸钠的质量为x,反应生成的氯化钠质量为y。
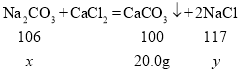
![]()
![]()
![]()
![]()
故纯碱样品中碳酸钠的质量为21.2g。
(2)反应后所得滤液中溶质的质量分数应当用反应后所有氯化钠质量除以反应后溶液总质量,因此反应后所得滤液中溶质的质量分数![]() 。
。

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目