题目内容
【题目】下列化学方程式书写正确的是
A.
B.
C.![]()
D.![]()
【答案】B
【解析】
书写化学方程式的步骤一般有四步:1.根据实验事实,在式子的左、右两边分别写出反应物和生成物的化学式,并在式子的左、右两边之间画一条短线;当反应物或生成物有多种时,中间用加号(即“+”)连接起来。2.配平化学方程式,并检查后,将刚才画的短线改写成等号(表示式子左、右两边每一种元素原子的总数相等)。3.标明化学反应发生的条件(因为化学反应只有在一定的条件下才能发生);如点燃、加热(常用“△”号表示)、催化剂、通电等。并且,一般都写在等号的上面,若有两个条件,等号上面写一个下面写一个。4.注明生成物中气体或固体的状态符号(即“↑”、“↓”);一般标注在气体或固体生成物的化学式的右边。但是,如果反应物和生成物中都有气体或固体时,其状态符号就不用标注了。
A. 镁燃烧生成氧化镁,方程式为:![]() ,选项错误;
,选项错误;
B. 氢气和氧气在点燃条件下生成水,方程式为: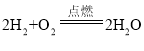 ,选项正确;
,选项正确;
C. 碳酸钙和盐酸反应生成氯化钙、二氧化碳、水,方程式为:![]() ,选项错误;
,选项错误;
D. 硫酸和铁反应生成硫酸亚铁和氢气,方程式为:![]() ,选项错误。
,选项错误。
故选B。

 阅读快车系列答案
阅读快车系列答案【题目】学习金属的化学性质时,老师给同学们做了锌与稀硫酸反应制取氢气的实验。有同学问老师:可以用锌与浓硫酸反应来制取氢气吗?老师让同学们先去查资料,然后对锌与浓硫酸反应产生的气体进行探究
(提出问题)锌与浓硫酸完全反应产生的气体是什么?
(查阅资料)
(1)浓硫酸是强氧化性酸,能与多数金属(如Mg、Zn、Cu等)反应产生SO2。
锌与浓硫酸反应:![]()
(2)SO2是一种有刺激性气味的有毒气体,与CO2有相似的化学性质,与Ca(OH)2反应产生不溶于水的CaSO3(提出猜想)猜想1:只有SO2 猜想2:H2和SO2 猜想3:_____。
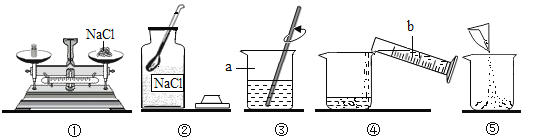
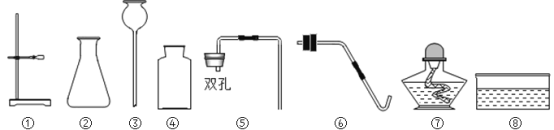
(实验探究)
同学们在老师指导下设计并进行如下图的实验:
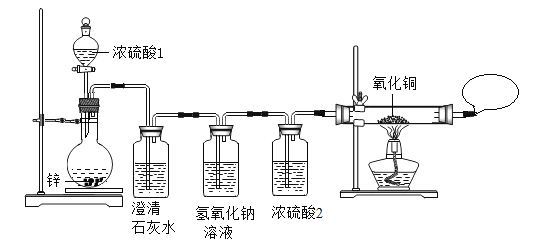
(现象与结论)
实验现象 | 实验结论 |
(1)_____。 | 有SO2产生。 |
(2)黑色的氧化铜变红色 | _____。 |
(得出结论)猜想_____正确。
(反思与拓展)
(1)实验中两处用了浓硫酸。浓硫酸2的作用是_____。
(2)有同学提出:实验进行到后阶段才能观察到黑色的氧化铜逐渐变红色。请解释实验开始阶段CuO处没有明显现象的原因:_____。
(3)实验室用金属与浓硫酸反应制取较纯的SO2气体,现有金属Zn和Cu最好选用金属_____理由是_____。
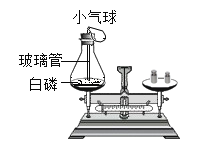
【题目】学习质量守恒定律后,某化学兴趣小组的同学利用如图所示的三个实验探究质量守恒定律。
[提出问题]化学反应前后各物质的质量总和是否相等?
[猜想假设]猜想1:不相等;猜想2:相等。
[实验探究]甲、乙、丙三组同学用托盘天平分别称量反应前后物质的质量。
实验方案 | 实验现象 | 结论 | |
甲组 |
| 产生大量气泡,天平指针向右偏转。 | 不相等。 导致甲组方案反 应前后质量不相等的原因是____________。 |
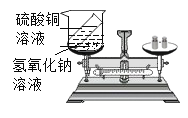
乙组 |
| 产生蓝色沉淀,天平指针_____________。(“向右偏转”、 “向左偏转”或“不发生偏转”) | 相等 |
丙组 |
| _____________, 天平指针没有发生偏转。 | 相等 |
[反思评价]在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在_____中进行。
[得出结论]甲组同学对装置进行改进后再次探究,亦能得出猜想2正确的结论。经同学们进一步讨论分析发现,反应体系中的反应仪器和未参加反应的物质质量在反应前后保持不变,最终得出结论是:_____________________的各物质的质量总和等于反应后生成的各物质的质量总和。
[微观解释]化学反应前后,原子的_______________________没有改变,原子的数目没有增减,原子的质量没有变化,所以质量守恒。