题目内容
下图是在一定量氢氧化钠溶液中不断加入盐酸的曲线图。纵坐标能表示的意义是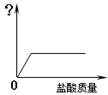
| A.溶液温度变化 | B.生成氯化钠的质量 |
| C.溶液中水的质量 | D.溶液中氯化氢的质量 |
B
解析

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案以下是我们日常生活中常用各种清洗剂,选择适当的用品可以得到更好的清洗效果。
| 名称 | 洗涤灵 | 洁厕灵 | 炉具清洁剂 | 污渍爆炸盐 | 漂白粉 |
| 产品样式 |  |  |  |  |  |
| 有效成分 或功能 | 清洗油污 | 盐酸 | 氢氧化钠 | 过碳酸钠 | 消毒 |
(2)以下物质可以使用洁厕灵清洗的是 填字母序号)。
a.铁锈 b.油渍 c.水垢(主要成分为碳酸钙和氢氧化镁)
(3)取上述一定量的炉具清洁剂,滴加几滴酚酞溶液,溶液变 色,若将洁厕灵与炉具清洁剂混合,可以发生下图所示的化学反应。图中a微粒的化学式为 。

(4)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2。将爆炸盐溶于水后,再加入足量的洁厕灵,发生的化学反应方程式为 。
(5)化学小组发现一袋包装破损的漂白粉,同学们对漂白粉其漂白作用是否失效产生了疑问。(当有效成分完全消失时,则漂白粉就完全失效;部分消失时,则为部分失效)。
I.查阅资料:
①漂白粉的主要成分是Ca(ClO)2、CaCl2和Ca(OH)2,其有效成分是Ca(ClO)2。
②Ca(ClO)2可溶于水,漂白原理是:它在空气中发生反应:
Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO。
③ HClO不稳定,易分解生成HCl和一种常见的单质气体。
④ CaCl2的水溶液呈中性,HClO的水溶液呈酸性。
⑤ HClO可使有色物质(如:品红溶液)褪色。
II.交流讨论:
该小组同学经过分析得出:HClO分解时除生成HCl外,生成的另一种常见气体是 。
III.实验探究:下表是探究某漂白粉是否完全失效的实验,请根据表中结论,进行填空。
| 实验步骤 | 实验现象 | 实验结论 |
| 把少量漂白粉样品加入水中,通入足量的CO2气体, 。 | 。 | 漂白粉的漂白作用已完全失效。 |
猜想一:CaCl2和CaCO3; 猜想二: ;
小明同学认为猜想中的成分CaCO3,除漂白粉的有效成分在空气中发生反应生成外,还有其它来源,请你用化学方程式表示 。
小聪同学进行实验证明失效后的漂白粉的成分符合猜想一,而与猜想二不符。小聪同学的实验方案是: 。
以下是我们日常生活中常用各种清洗剂,选择适当的用品可以得到更好的清洗效果。
| 名称 | 洗涤灵 | 洁厕灵 | 炉具清洁剂 | 污渍爆炸盐 | 漂白粉 |
| 产品样式 |
|
|
|
|
|
| 有效成分 或功能 | 清洗油污 | 盐酸 | 氢氧化钠 | 过碳酸钠 | 消毒 |
(1)我们使用洗涤灵清洗餐具上的油污,这是因为它具有 的功能。
(2)以下物质可以使用洁厕灵清洗的是 填字母序号)。
a.铁锈 b.油渍 c.水垢(主要成分为碳酸钙和氢氧化镁)
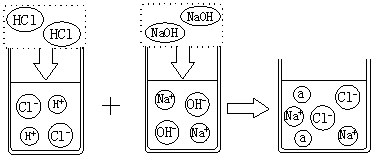 (3)取上述一定量的炉具清洁剂,滴加几滴酚酞溶液,溶液变 色,若将洁厕灵与炉具清洁剂混合,可以发生下图所示的化学反应。图中a微粒的化学式为 。
(3)取上述一定量的炉具清洁剂,滴加几滴酚酞溶液,溶液变 色,若将洁厕灵与炉具清洁剂混合,可以发生下图所示的化学反应。图中a微粒的化学式为 。
(4)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2。将爆炸盐溶于水后,再加入足量的洁厕灵,发生的化学反应方程式为 。
(5)化学小组发现一袋包装破损的漂白粉,同学们对漂白粉其漂白作用是否失效产生了疑问。(当有效成分完全消失时,则漂白粉就完全失效;部分消失时,则为部分失效)。
I.查阅资料:
①漂白粉的主要成分是Ca(ClO)2、CaCl2和Ca(OH)2,其有效成分是Ca(ClO)2。
②Ca(ClO)2可溶于水,漂白原理是:它在空气中发生反应: Ca(ClO)2+H![]() 2O+CO2=CaCO3↓+2HClO。
2O+CO2=CaCO3↓+2HClO。
③ HClO不稳定,易分解生成HCl和一种常见的单质气体。
④ CaCl2的水溶液呈中性,HClO的水溶液呈酸性。
⑤ HClO可使有色物质(如:品红溶液)褪色。
II.交流讨论:
该小组同学经过分析得出:HClO分解时除生成HCl外,生成的另一种常见气体是 。
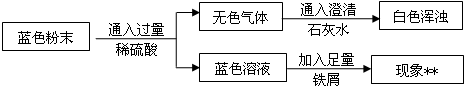
III.实验探究: 下表是探究某漂白粉是否完全失效的实验,请根据表中结论,进行填空。
| 实验步骤 | 实验现象 | 实验结论 |
| 把少量漂白粉样品加入水中,通入足量的CO2气体, 。 | 。 | 漂白粉的漂白作用已完全失效。 |
IV.继续探究:同学们对某完全失效后的漂白粉的成分很感兴趣,并作进一步探究。在老师的帮助下,同学们对该![]() 失效后的漂白粉成分进行猜想:
失效后的漂白粉成分进行猜想:
猜想一:CaCl2和CaCO3; 猜想二: ;
小明同学认为猜想中的成分CaCO3,除漂白粉的有效成分在空气中发生反应生成外,还有其它来源,请你用化学方程式表示 。
小聪同学进行实验证明失效后的漂白粉的成分符合猜想一,而与猜想二不符。小聪同学的实验方案:
 锥形瓶及其中各物质的总质量、
锥形瓶及其中各物质的总质量、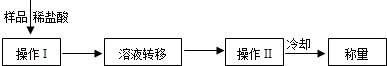
 锥形瓶及其中各物质的总质量、________.该方案有误差,请写出引起误差的一个原因:________.
锥形瓶及其中各物质的总质量、________.该方案有误差,请写出引起误差的一个原因:________.




 ]
]